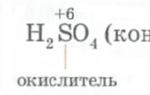Свинец в природе. Значение для людей прошлого и применение
Свинец (Pb от лат. Plumbum) – химический элемент, который находится в IV группе Таблицы Менделеева. Свинец имеет множество изотопов, среди которых более 20 обладают радиоактивными свойствами. Изотопы свинца являются продуктами распада урана и тория, поэтому содержание свинца в литосфере постепенно увеличивалось в течение миллионов лет и сейчас составляет около 0,0016% по массе, но он более распространен, чем его ближайшие родственники, такие как золото и . Свинец легко выделяется из рудных месторождений. Основные источники свинца - галенит, англезит и церуссит. В руде со свинцом очень часто соседствуют другие металлы, например, цинк , кадмий и висмут. В самородном виде свинец встречается исключительно редко.
Свинец - интересные исторические факты
Этимология слова «свинец» до сих пор точно не выяснена и является предметом очень интересных исследований. Свинец очень похож на олово, очень часто их путали, поэтому в большинстве западнославянских языков свинец это олово. Зато слово «свинец» встречается в литовском (svinas) и латышском (svin) языках. Свинец в переводе на английский lead, на голландский lood. Видимо отсюда и пошло слово «лудить», т.е. покрывать изделие слоем олова (или свинца). Не до конца понятно также происхождение латинского слова Plumbum, от которого произошло английское слово plumber – водопроводчик. Дело в том, что когда-то водопроводные трубы «запечатывали» свинцом, «пломбировали» (франц. plomber «запечатывать свинцом»). Кстати, отсюда же всем известное слово «пломба». Но на этом путаница не заканчивается, греки всегда называли свинец «молибдос», отсюда и латинское «molibdaena», незнающему человеку легко спутать это название с наименованием химического элемента молибден . Так в древности называли блестящие минералы оставляющие тёмный след на светлой поверхности. Этот факт оставил свой след в немецком языке: «карандаш» по-немецки называется Bleistift, т.е. свинцовый стержень.
Человечество знакомо со свинцом с незапамятных времен. Археологами найдены свинцовые изделия выплавленные 8000 лет тому назад. В Древнем Египте из свинца даже отливали статуи. В Древнем Риме из свинца были изготовлены водопроводные трубы, именно он предопределил первую в истории экологическую катастрофу. Римляне не имели никакого представления о вреде свинца, им нравился податливый, прочный и простой в работе металл. Считалось даже, что свинец, добавленный в вино, улучшает его вкус. Поэтому почти каждый римлянин был отравлен свинцом. О симптомах отравления свинцом мы расскажем ниже, а пока лишь укажем, что одним из них является расстройство рассудка. Видимо отсюда и берут свое начало все эти безумные выходки знатных римлян и бесчисленные сумасшедшие оргии. Некоторые исследователи даже считают, что свинец явился чуть ли основной причиной падения Древнего Рима.
В древности гончары мололи свинцовую руду, разводили водой и обливали полученной смесью глиняные предметы. После обжига такие сосуды покрывались тонким слоем блестящего свинцового стекла.
Англичанин Джордж Равенскрофт в 1673 году усовершенствовал состав стекла, добавив к исходным компонентам оксид свинца и таким образом получил легкоплавкое блестящее стекло, которое было очень похоже на натуральный горный хрусталь. А в конце 18 века Георг Страсс при производстве стекла сплавил вместе белый песок, поташ и оксид свинца, получив такое чистое и блестящее стекло, что его сложно было отличить от алмаза. Отсюда и пошло название «стразы», по сути подделка под драгоценные камни. К сожалению, среди современников Страсс прослыл мошенником и его изобретение находилось в забвении до тех пор, пока в начале XX века Даниэль Сваровски не смог сделать из производства страз целую индустрию моды и направление искусства.
После появления и широкого распространения огнестрельного оружия, свинец начал использоваться для производства пуль и дроби. Из свинца изготавливали типографские литеры. Свинец ранее входил в состав белой и красной красок, ими писали почти все старинные художники.
Свинцовая дробь
Химические свойства свинца кратко
Свинец - металл матового серого цвета. Однако его свежий срез хорошо блестит, но к сожалению почти моментально покрывается грязноватой оксидной плёнкой. Свинец очень тяжелый металл, он тяжелее железа в полтора раза, а алюминия в четыре. Недаром в русском языке слово «свинцовый» является в некоторой мере синонимом тяжести. Свинец очень легкоплавкий металл, он плавится уже при 327 ° С. Ну, этот факт известен всем рыбакам, которые с легкостью выплавляют нужные по весу грузила. Также свинец очень мягок, его можно резать обычным стальным ножом. Свинец очень малоактивный металл, провести с ним реакцию или растворить его не составляет никакого труда даже при комнатной температуре.
Органические производные свинца являются очень ядовитыми веществами. К сожалению, одно из них, тетраэтилсвинец, широко использовалось как присадка к бензину, позволяющая повысить октановое число. Но зато к счастью, тетраэтилсвинец больше не применяется в такой ипостаси, химики и производственники научились повышать октановое число более безопасными способами.
Влияние свинца на организм человека и симптомы отравления
Любые соединения свинца очень ядовиты. Металл проникает в организм вместе с едой или со вдыхаемым воздухом и разносится кровью. Причем вдыхание паров свинцовых соединений и пыли намного более опасно, чем присутствие его в пище. Свинец имеет свойство накапливаться в костях, частично замещая в этом случае кальций . При повышении концентрации свинца в организме развивается анемия, поражается головной мозг, что приводит к снижению интеллекта, а у детей может вызвать необратимые задержки в развитии. Достаточно растворить один миллиграмм свинца в литре воды и она станет не только непригодной, но и опасной для питья. Такое низкое количество свинца представляет также определенную опасность, ни цвет ни вкус воды не изменяется. Основные симптомы отравления свинцом:
- серая кайма на деснах,
- вялость,
- апатия,
- потеря памяти,
- слабоумие,
- проблемы со зрением,
- раннее старение.
Применение свинца
Всё же, несмотря на токсичность, отказаться от использования свинца пока нет никакой возможности ввиду его исключительных свойств и дешевизны. Свинец в основном используется для производства аккумуляторных пластин, на эти нужды в настоящее время тратится около 75% добываемого на планете свинца. Свинец используется как оболочка для электрических кабелей, благодаря своей пластичности и неподверженности коррозии. Этот металл широко используется в химической и нефтеперерабатывающей промышленности, например, для облицовки реакторов в которых получают серную кислоту. Свинец обладает свойством задерживать радиоактивное излучение, этим тоже широко пользуются в энергетике, медицине и химии. В свинцовых контейнерах, к примеру, транспортируют радиоактивные элементы. Свинец идет в производство сердечников пуль и шрапнели. Также этот металл находит свое применение в производстве подшипников.
 Свинцовая статуя Святого Мартина в Братиславе
Свинцовая статуя Святого Мартина в Братиславе
СВИНЕЦ, Pb (лат. plumbum * а. lead, plumbum; н. Blei; ф. plomb; и. plomo), — химический элемент IV группы периодической системы Менделеева , атомный номер 82, атомная масса 207,2. Природный свинец представлен четырьмя стабильными 204 Pb (1,48%), 206 Pb (23,6%), 207 Pb (22,6%) и 208 Pb (52,3%) и четырьмя радиоактивными 210 Pb, 211 Pb, 212 Pb и 214 Pb изотопами; кроме того, получено более десяти искусственных радиоактивных изотопов свинца. Известен с древних времён.
Физические свойства
Свинец — мягкий пластичный синевато-серый металл; кристаллическая решётка кубическая гранецентрированная (а=0,49389 нм). Атомный радиус свинца 0,175 нм, ионный радиус 0,126 нм (Pb 2+) и 0,076 нм (Pb 4+). Плотность 11 340 кг/м 3 , t плавления 327,65°С, t кипения 1745°С, теплопроводность 33,5 Вт/(м.град), теплоёмкость Cp° 26,65 Дж/(моль.К), удельное электрическое сопротивление 19,3.10 -4 (Ом.м), температурный коэффициент линейного расширения 29,1.10 -6 К -1 при 20°С. Свинец диамагнитен, при 7,18 К становится сверхпроводником.
Химические свойства свинца
Степень окисления +2 и +4. Свинец сравнительно мало химически активен. На воздухе свинец довольно быстро покрывается тонкой плёнкой оксида, предохраняющей его от дальнейшего окисления. Хорошо реагирует с азотной и уксусной кислотами, растворами щелочей, не взаимодействует с соляной и серной кислотами. При нагревании свинец взаимодействует с галогенами, серой , селеном , таллием . Азид свинца Pb(N 3) 2 разлагается при нагревании или ударе со взрывом . Соединения свинца токсичны , ПДК 0,01 мг/м 3 .
Среднее содержание (кларк) свинца в земной коре 1,6.10 -3 % по массе, при этом ультраосновные и основные горные породы содержат меньше свинца (1.10 -5 и 8.10 -3 % соответственно), чем кислые (10 -3 %); в осадочных горных породах — 2.10 -3 %. Свинец накапливается главным образом в результате гидротермальных и гипергенных процессов, нередко образуя крупные месторождения. Существует более 100 минералов свинца, среди которых наиболее важное значение имеют галенит (PbS), церуссит (PbCО 3), англезит (PbSО 4). Одна из особенностей свинца состоит в том, что из четырёх стабильных изотопов один (204 Pb) нерадиогенный и, следовательно, количество его остаётся постоянным, а три других (206 Pb, 207 Pb и 208 Pb) — конечные продукты радиоактивного распада 238 U, 235 U и 232 Th соответственно, вследствие чего их количество постоянно возрастает. Изотопный состав Pb Земли за 4,5 млрд. лет изменился от первичного 204 Pb (1,997%), 206 Pb (18,585%), 207 Pb (20,556%), 208 Pb (58,861%) до современного 204 Pb (1,349%), 206 Pb (25,35%), 207 Pb (20,95%), 208 Pb (52,349%). Изучая изотопный состав свинца в горных породах и рудах , можно устанавливать генетические соотношения, решать разнообразные вопросы геохимии , геологии , тектоники отдельных регионов и Земли в целом и т.д. Изотопные исследования свинца применяются и в поисково-разведочных работах. Широкое развитие получили также методы U-Th-Pb геохронологии , основанные на изучении количественных соотношений между материнскими и дочерними изотопами в горных породах и минералах. В биосфере свинец рассеян, его очень мало в живом веществе (5.10 -5 %) и в морской воде (3.10 -9 %). В промышленно развитых странах концентрация свинца в воздухе, особенно вблизи автомобильных дорог с интенсивным движением, резко возрастает, достигая в отдельных случаях опасных содержаний для здоровья людей.
Получение и применение
Металлический свинец получают окислительным обжигом сульфидных руд с последующим восстановлением PbO до чернового металла и рафинированием последнего. В черновом свинца содержится до 98% Pb, в рафинированном — 99,8-99,9%. Дальнейшая очистка свинца до значений, превышающих 99,99%, проводится с помощью электролиза. Для получения особо чистого металла применяют методы амальгамации , зонной перекристаллизации и др.
Свинец широко применяется в производстве свинцовых аккумуляторов, для изготовления аппаратуры, устойчивой в агрессивных средах и газах. Из свинца изготавливают оболочки электрических кабелей и различные сплавы. Широкое применение нашёл свинец при изготовлении средств защиты от ионизирующих излучений. Оксид свинца добавляют в шихту при производстве хрусталя. Соли свинца используются при производстве красителей, азид свинца — как инициирующее взрывчатое вещество , а тетраэтилсвинец Pb(С 2 Н 5) 4 — как антидетонатор горючего для двигателей внутреннего сгорания.
Свинец - во многом идеальный металл, ведь он обладает массой важных для промышленности достоинств. Наиболее очевидное из них - сравнительная легкость его получения из руд, которая объясняется низкой температурой плавления (всего 327°С). При обработке важнейшей свинцовой руды - галенита, - металл легко отделяется от серы. Для этого галенит достаточно в смеси с углем обжечь на воздухе..
Из-за высокой пластичности свинец легко куется, прокатывается в листы и проволоку, что позволяет применять его в машиностроительной промышленности для изготовления различных сплавов с другими металлами. Широкой известностью пользуются так называемые баббиты (подшипниковые сплавы свинца с оловом, цинком и некоторыми другими металлами), типографские сплавы свинца с сурьмой и оловом, сплавы свинца с оловом для пайки различных металлов.
Металлический свинец - очень хорошая защита от всех видов радиоактивного излучения и рентгеновских лучей. Он введен в резину фартука и защитных рукавиц врача-рентгенолога, задерживая рентгеновские лучи и предохраняя организм от их губительного действия. Защищает от радиоактивного излучения и стекло, содержащее окислы свинца. Подобное свинцовое стекло позволяет управлять обработкой радиоактивных материалов с помощью "механической руки" - манипулятора.
При воздействии воздуха, воды и различных кислот свинец проявляет большую устойчивость. Это свойство позволяет широко использовать его в электротехнической промышленности, особенно для изготовления аккумуляторов и кабельных рубок. Последние находят широкое применение в авиа- и радиопромышленности. Устойчивость свинца позволяет использовать его и для предохранения от порчи медных проводов телеграфных и телефонных линий. Тонкими свинцовыми листами покрывают железные и медные детали, подвергающиеся химическому воздействию (ванны для электролиза меди, цинка и других металлов).
Свинец и электротехникаОсобенно много свинца потребляет кабельная промышленность, где им предохраняют от коррозии телеграфные и электрические провода при подземной или подводной прокладке. Много свинца идет и на изготовление легкоплавких сплавов (с висмутом, оловом и кадмием) для электрических предохранителей, а также для точной пригонки контактирующих деталей. Но главное, видимо, – это использование свинца в химических источниках тока.
Свинцовый аккумулятор с момента своего создания претерпел много конструктивных изменений, но основа его осталась той же: две свинцовые пластины, погруженные в сернокислый электролит. На пластины нанесена паста из окиси свинца. При зарядке аккумулятора на одной из пластин выделяется водород, восстанавливающий окись до металлического свинца, на другой – кислород, переводящий окись в перекись. Вся конструкция превращается в гальванический элемент с электродами из свинца и перекиси свинца. В процессе разрядки перекись раскисляется, а металлический свинец превращается в окись. Эти реакции сопровождаются возникновением электрического тока, который будет течь по цепи до тех пор, пока электроды не станут одинаковыми – покрытыми окисью свинца.
Производство щелочных аккумуляторов достигло в наше время гигантских размеров, но оно не вытеснило аккумуляторы свинцовые. Последние уступают щелочным в прочности, они тяжелее, но зато дают ток большего напряжения. Так, для питания автостартера нужно пять кадмиево-никелевых аккумуляторов или три свинцовых.
Аккумуляторная промышленность – один из самых емких потребителей свинца.
Можно, пожалуй, сказать и то, что свинец находился у истоков современной электронно-вычислительной техники.
Свинец был одним из первых металлов, переведенных в состояние сверхпроводимости. Кстати, температура, ниже которой этот металл приобретает способность пропускать электрический ток без малейшего сопротивления, довольно высока – 7,17°K. (Для сравнения укажем, что у олова она равна 3,72, у цинка – 0,82, у титана – всего 0,4°K). Из свинца была сделана обмотка первого сверхпроводящего трансформатора, построенного в 1961 г.
На сверхпроводимости свинца основан один из самых эффектных физических «фокусов», впервые продемонстрированный в 30-х годах советским физиком В.К. Аркадьевым.
По преданию, гроб с телом Магомета висел в пространстве без опор. Из трезвомыслящих людей никто, конечно, этому не верит. Однако в опытах Аркадьева происходило нечто подобное: небольшой магнитик висел без какой-либо опоры над свинцовой пластинкой, находившейся в среде жидкого гелия, т.е. при температуре 4,2°K, намного меньшей, чем критическая для свинца.
Известно, что при изменении магнитного поля в любом проводнике возникают вихревые токи (токи Фуко). В обычных условиях они быстро гасятся сопротивлением. Но, если сопротивления нет (сверхпроводимость!), эти токи не затухают и, естественно, сохраняется созданное ими магнитное поле. Магнитик над свинцовой пластинкой имел, разумеется, свое поле и, падая на нее, возбуждал магнитное поле от самой пластинки, направленное навстречу полю магнита, и оно отталкивало магнит. Значит, задача сводилась к тому, чтобы подобрать магнитик такой массы, чтобы его могла удержать на почтительном расстоянии эта сила отталкивания.
В наше время сверхпроводимость – огромнейшая область научных исследований и практического приложения. Говорить о том, что она связана только со свинцом, конечно нельзя. Но значение свинца в этой области не исчерпывается приведенными примерами.
Один из лучших проводников электричества – медь – никак не удается перевести в сверхпроводящее состояние. Почему это так, у ученых еще нет единого мнения. В экспериментах по сверхпроводимости меди отведена роль электроизолятора. Но сплав меди со свинцом используют в сверхпроводниковой технике. В температурном интервале 0,1...5°K этот сплав проявляет линейную зависимость сопротивления от температуры. Поэтому его используют в приборах для измерения исключительно низких температур.
Свинец и транспортИ эта тема складывается из нескольких аспектов. Первый – это антифрикционные сплавы на основе свинца. Наряду с общеизвестными баббитами и свинцовыми бронзами, антифрикционным сплавом часто служит свинцово-кальциевая лигатура (3...4% кальция). То же назначение имеют и некоторые припои, отличающиеся низким содержанием олова и, в отдельных случаях, добавкой сурьмы. Все более важную роль начинают играть сплавы свинца с таллием. Присутствие последнего повышает теплостойкость подшипников, уменьшает коррозию свинца органическими кислотами, образующимися при физико-химическом разрушении смазочных масел.
Второй аспект – борьба с детонацией в двигателях. Процесс детонации сродни процессу горения, но скорость его слишком велика... В двигателях внутреннего сгорания он возникает из-за распада молекул еще не сгоревших углеводородов под влиянием растущих давления и температуры. Распадаясь, эти молекулы присоединяют кислород и образуют перекиси, устойчивые лишь в очень узком интервале температур. Они-то и вызывают детонацию, и топливо воспламеняется раньше, чем достигнуто необходимое сжатие смеси в цилиндре. В результате мотор начинает «барахлить», перегреваться, появляется черный выхлоп (признак неполного сгорания), ускоряется выгорание поршней, сильнее изнашивается шатунно-кривошипный механизм, теряется мощность...
Самый распространенный антидетонатор – тетраэтилсвинец (ТЭС) Pb(С 2 Н 5) 4 – бесцветная ядовитая жидкость. Действие ее (и других металлоорганических антидетонаторов) объясняется тем, что при температуре выше 200°C происходит распад молекул вещества-антидетонатора. Образуются активные свободные радикалы, которые, реагируя прежде всего с перекисями, уменьшают их концентрацию. Роль металла, образующегося при полном распаде тетраэтилсвинца, сводится к дезактивации активных частиц – продуктов взрывного распада тех же перекисей.
Добавка тетраэтилсвинца к топливу никогда не превышает 1%, но не только из-за токсичности этого вещества. Избыток свободных радикалов может инициировать образование перекисей.
Важная роль в изучении процессов детонации моторных топлив и механизма действия антидетонаторов принадлежит ученым Института химической физики АН СССР во главе с академиком Н.Н. Семеновым и профессором А.С. Соколиком.
Свинец и войнаСвинец – тяжелый металл, его плотность 11,34. Именно это обстоятельство послужило причиной массового использования свинца в огнестрельном оружии. Между прочим, свинцовыми метательными снарядами пользовались еще в древности: пращники армии Ганнибала метали в римлян свинцовые шары. И сейчас пули отливают из свинца, лишь оболочку их делают из других, более твердых металлов.
Любая добавка к свинцу увеличивает его твердость, но количественно влияние добавок неравноценно. В свинец, идущий на изготовление шрапнели, добавляют до 12% сурьмы, а в свинец ружейной дроби – не более 1% мышьяка.
Без инициирующих взрывчатых веществ ни одно скорострельное оружие действовать не будет. Среди веществ этого класса преобладают соли тяжелых металлов. Используют, в частности, азид свинца PbN 6 .
Ко всем взрывчатым веществам предъявляют очень жесткие требования с точки зрения безопасности обращения с ними, мощности, химической и физической стойкости, чувствительности. Из всех известных инициирующих взрывчатых веществ по всем этим характеристикам «проходят» лишь «гремучая ртуть», азид и тринитрорезорцинат свинца (ТНРС).
Свинец и наукаВ Аламогордо – место первого атомного взрыва – Энрико Ферми выехал в танке, оборудованном свинцовой защитой. Чтобы понять, почему от гамма-излучения защищаются именно свинцом, нам необходимо обратиться к сущности поглощения коротковолнового излучения.
Гамма-лучи, сопровождающие радиоактивный распад, идут из ядра, энергия которого почти в миллион раз превышает ту, что «собрана» во внешней оболочке атома. Естественно, что гамма-лучи неизмеримо энергичнее лучей световых. Встречаясь с веществом, фотон или квант любого излучения теряет свою энергию, этим-то и выражается его поглощение. Но энергия лучей различна. Чем короче их волна, тем они энергичнее, или, как принято выражаться, жестче. Чем плотнее среда, через которую проходят лучи, тем сильнее она их задерживает. Свинец плотен. Ударяясь о поверхность металла, гамма-кванты выбивают из нее электроны, на что расходуют свою энергию. Чем больше атомный номер элемента, тем труднее выбить электрон с его внешней орбиты из-за большей силы притяжения ядром.
Возможен и другой случай, когда гамма-квант сталкивается с электроном, сообщает ему часть своей энергии и продолжает свое движение. Но после встречи он стал менее энергичным, более «мягким», и в дальнейшем слою тяжелого элемента поглотить такой квант легче. Это явление носит название комптон-эффекта по имени открывшего его американского ученого.
Чем жестче лучи, тем больше их проникающая способность – аксиома, не требующая доказательств. Однако ученых, положившихся на эту аксиому, ожидал весьма любопытный сюрприз. Вдруг выяснилось, что гамма-лучи энергией более 1 млн эВ задерживаются свинцом не слабее, а сильнее менее жестких! Факт, казалось, противоречащий очевидности. После проведения тончайших экспериментов выяснилось, что гамма-квант энергией более 1,02 МэВ в непосредственной близости от ядра «исчезает», превращаясь в пару электрон – позитрон, и каждая из частиц уносит с собой половину затраченной на их образование энергии. Позитрон недолговечен и, столкнувшись с электроном, превращается в гамма-квант, но уже меньшей энергии. Образование электронно-позитронных пар наблюдается только у гамма-квантов высокой энергии и только вблизи от «массивного» ядра, то есть в элементе с бóльшим атомным номером.
Свинец – один из последних стабильных элементов таблицы Менделеева. И из тяжелых элементов – самый доступный, с отработанной веками технологией добычи, с разведанными рудами. И очень пластичный. И очень удобный в обработке. Вот почему свинцовая защита от излучения – самая распространенная. Пятнадцати-двадцати-сантиметрового слоя свинца достаточно, чтобы предохранить людей от действия излучения любого известного науке вида.
Коротко упомянем еще об одной стороне служения свинца науке. Она тоже связана с радиоактивностью.
В часах, которыми мы пользуемся, нет свинцовых деталей. Но в тех случаях, когда время измеряют не часами и минутами, а миллионами лет, без свинца не обойтись. Радиоактивные превращения урана и тория завершаются образованием стабильных изотопов элемента №82. При этом, правда, получается разный свинец. Распад изотопов 235 U и 238 U приводит в конечном итоге к изотопам 207 Pb и 206 Pb. Наиболее распространенный изотоп тория 232 Th заканчивает свои превращения изотопом 208 Pb. Установив соотношение изотопов свинца в составе геологических пород, можно узнать, сколько времени существует тот или иной минерал. При наличии особо точных приборов (масс-спектрометров) возраст породы устанавливают по трем независимым определениям – по соотношениям 206 Pb: 238 U; 207 Pb: 235 U и 208 Pb: 232 Th.
Свинец и культураНачнем с того, что эти строчки отпечатаны литерами, изготовленными из свинцового сплава. Главные компоненты типографских сплавов – свинец, олово и сурьма. Интересно, что свинец и олово стали использовать в книгопечатании с первых его шагов. Но тогда они не составляли единого сплава. Немецкий первопечатник Иоганн Гуттенберг литеры из олова отливал в свинцовые формы, так как считал удобным чеканить из мягкого свинца формы, которые выдерживали определенное количество заливок олова. Нынешние оловянно-свинцовые типографские сплавы составляют так, чтобы они удовлетворяли многим требованиям: они должны иметь хорошие литьевые свойства и незначительную усадку, быть достаточно твердыми и химически стойкими по отношению к краскам и смывающим их растворам; при переплавке должно сохраняться постоянство состава.
Однако служение свинца человеческой культуре началось задолго до появления первых книг. Живопись появилась раньше письменности. На протяжении многих столетий художники использовали краски на свинцовой основе, и они до сих пор не вышли из употребления: желтая – свинцовый крон, красная – сурик и, конечно, свинцовые белила. Между прочим, именно из-за свинцовых белил кажутся темными картины старых мастеров. Под действием микропримесей сероводорода в воздухе свинцовые белила превращаются в темный сернистый свинец PbS...
С давних пор стенки гончарных изделий покрывали глазурями. Простейшая глазурь делается из окиси свинца и кварцевого песка. Ныне санитарный надзор запрещает использовать эту глазурь при изготовлении предметов домашнего обихода: контакт пищевых продуктов с солями свинца должен быть исключен. Но в составе майоликовых глазурей, предназначенных для декоративных целей, сравнительно легкоплавкие соединения свинца используют, как и прежде.
Наконец, свинец входит в состав хрусталя, точнее, не свинец, а его окись. Свинцовое стекло варится без каких-либо осложнений, оно легко выдувается и гранится, сравнительно просто нанести на него узоры и обычную нарезку, винтовую, в частности. Такое стекло хорошо преломляет световые лучи и потому находит применение в оптических приборах.
Добавляя в шихту свинец и поташ (вместо извести), приготовляют страз – стекло с блеском, большим, чем у драгоценных камней.
Свинец и медицинаПопадая в организм, свинец, как и большинство тяжелых металлов, вызывает отравления. И тем не менее свинец нужен медицине. Со времен древних греков остались во врачебной практике свинцовые примочки и пластыри, но этим не ограничивается медицинская служба свинца.
Желчь нужна не только сатирикам. Содержащиеся в ней органические кислоты, прежде всего гликохолевая C 23 H 36 (OH) 3 CONHCH 2 COOH, а также таурохолевая C 23 H 36 (OH) 3 CONHCH 2 CH 2 SO 3 H, стимулируют деятельность печени. А поскольку не всегда и не у всех печень работает с точностью хорошо отлаженного механизма, эти кислоты нужны медицине. Выделяют их и разделяют с помощью уксуснокислого свинца. Свинцовая соль гликохолевой кислоты выпадает при этом в осадок, а таурохолевой – остается в маточном растворе. Отфильтровав осадок, из маточного раствора выделяют и второй препарат, действуя опять же свинцовым соединением – основной уксусной солью.
Но главная работа свинца в медицине связана с диагностикой и рентгенотерапией. Он защищает врачей от постоянного рентгеновского облучения. Для практически полного поглощения лучей Рентгена достаточно на их пути поставить слой свинца в 2...3 мм. Вот почему медицинский персонал рентгеновских кабинетов облачен в фартуки, рукавицы и шлемы из резины, в состав которой введен свинец. И изображение на экране наблюдают через свинцовое стекло.
Таковы главные аспекты взаимоотношений человечества со свинцом – элементом, известным с глубокой древности, но и сегодня служащим человеку во многих областях его деятельности.
Чудесные горшки благодаря свинцу
Производство металлов, прежде всего золота, в Древнем Египте считалось «священным искусством». Завоеватели Египта истязали его жрецов, выпытывая у них секреты выплавки золота, но те умирали, сохраняя тайну. Сущность процесса, который египтяне так оберегали, выяснили спустя много лет. Они обрабатывали золотую руду расплавленным свинцом, растворяющим благородные металлы, и таким образом извлекали золото из руд. Этот раствор затем подвергали окислительному обжигу, и свинец превращался в окись. Главной тайной этого процесса были горшки для обжига. Их делали из костяной золы. При плавке окись свинца впитывалась в стенки горшка, увлекая при этом случайные примеси. А на дне оставался чистый сплав.
Использование свинцового балласта
26 мая 1931 г. профессор Огюст Пиккар должен был подняться в небо на стратостате собственной конструкции – с герметичной кабиной. И поднялся. Но, разрабатывая детали предстоящего полета, Пиккар неожиданно столкнулся с препятствием совсем не технического порядка. В качестве балласта он решил взять на борт не песок, а свинцовую дробь, для которой требовалось гораздо меньше места в гондоле. Узнав об этом, чиновники, ведавшие полетом, категорически запретили замену: в правилах сказано «песок», ничто другое сбрасывать на головы людей недопустимо (за исключением лишь воды). Пиккар решил доказать безопасность своего балласта. Он вычислил силу трения свинцовой дроби о воздух и распорядился сбросить эту дробь ему на голову с самой высокой постройки Брюсселя. Полная безопасность «свинцового дождя» была доказана наглядно. Однако администрация оставила опыт без внимания: «Закон есть закон, сказано песок, значит, песок, а не дробь». Препятствие казалось неодолимым, но ученый нашел выход: он объявил, что в гондоле стратостата в качестве балласта будет находиться «свинцовый песок». Заменой слова «дробь» на слово «песок» бюрократы были обезоружены и более не препятствовали Пиккару.
Свинец в лакокрасочной промышленности
Свинцовые белила умели изготовлять 3 тыс. лет назад. Основным поставщиком их в древнем мире был остров Родос в Средиземном море. Красок тогда не хватало, и стоили они чрезвычайно дорого. Прославленный греческий художник Никий однажды с нетерпением ожидал прибытия белил с Родоса. Драгоценный груз прибыл в афинский порт Пирей, но там неожиданно вспыхнул пожар. Пламя охватило корабли, на которых были привезены белила. Когда пожар погасили, расстроенный художник поднялся на палубу одного из пострадавших кораблей. Он надеялся, что не весь груз погиб, мог же уцелеть хотя бы один бочонок с нужной ему краской. Действительно, в трюме нашлись бочки с белилами: они не сгорели, но сильно обуглились. Когда бочки вскрыли, то удивлению художника не было границ: в них была не белая краска, а ярко-красная! Так пожар в порту подсказал путь изготовления замечательной краски – сурика.
Свинец и газы
При плавке того или иного металла приходится заботиться об удалении из расплава газов, так как иначе получается низкокачественный материал. Добиваются этого различными технологическими приемами. Выплавка же свинца в этом смысле никаких хлопот металлургам не доставляет: кислород, азот, сернистый газ» водород, окись углерода, углекислый газ, углеводороды не растворяются ни в жидком, ни в твердом свинце.
Свинец в строительстве
В древности при строительстве зданий или оборонительных сооружений камни нередко скрепляли расплавленным свинцом. В селении Старый Крым и сейчас сохранились руины так называемой свинцовой мечети, сооруженной в XIV столетии. Такое название здание получило оттого, что зазоры в каменной кладке залиты свинцом.
Ограничения в применении свинца
В настоящее время промышленность всего мира переживает очередной этап преобразований, связанных с ужесточением экологических стандартов - происходит всеобщий отказ от свинца. Германия существенно ограничила его использование с 2000 г., Голландия - с 2002 г., а такие европейские страны, как Дания, Австрия и Швейцария, вообще запретили использование свинца. Эта тенденция станет общей для всех стран ЕС в 2015 г. США и Россия также активно развивают технологии, которые помогут найти альтернативу применению свинца.
Его широкое применение в промышленности привело к тому, что свинцовое загрязнение можно обнаружить повсюду. Рассмотрим важнейшие составляющие биосферы, такие как воздух, вода и почва.
Начнем с атмосферы. С воздухом в организм человека поступает незначительное количество свинца - (всего 1-2%), но при этом большая часть свинца усваивается. Наибольшие выбросы свинца в атмосферу происходят в следующих отраслях производства:
- металлургическая промышленность;
- машиностроение (производство аккумуляторов);
- топливно-энергетический комплекс (производство этилированного бензина);
- химический комплекс (производство пигментов, смазок и др.);
- стекольные предприятия;
- консервное производство;
- деревообрабатывающая и целлюлозно-бумажная промышленность;
- предприятия оборонной промышленности.
Без сомнения, наиболее значимым источником загрязнения атмосферы свинцом является автомобильный транспорт, использующий этилированный бензин.
Доказано, что повышение содержания свинца в питьевой воде обуславливает, как правило, увеличение его концентрации в крови. Значительное повышение содержания этого металла в поверхностных водах связано с его высокой концентрацией в сточных водах рудообогатительных фабрик, некоторых металлургических заводов, шахт и т.д.
Из загрязненной почвы свинец поступает в сельскохозяйственные культуры, а вместе с пищей - и непосредственно в организм человека. Отмечено активное накопление данного металла в капусте и корнеплодах, причем именно в тех, которые повсеместно употребляются в пищу (например, в картофеле). Некоторые виды почв прочно связывают свинец, что предохраняет от загрязнения грунтовые и питьевые воды, растительную продукцию. Но тогда сама почва постепенно становится все более зараженной и в какой-то момент может произойти разрушение органического вещества почвы с выбросом свинца в почвенный раствор. В итоге она окажется непригодной для сельскохозяйственного использования.
Таким образом, вследствие глобального загрязнения окружающей среды свинцом, он стал вездесущим компонентом любой растительной и животной пищи. В организм человека большая часть свинца поступает с продуктами питания - от 40 до 70% в разных странах. Растительные продукты в целом содержат больше свинца, чем животные.
Как уже было сказано, всему виною промышленные предприятия. Естественно, на самих производствах, имеющих дело со свинцом, экологическая обстановка хуже, чем где бы то ни было. По результатам официальной статистики, среди профессиональных интоксикаций свинцовая занимает первое место. В электротехнической промышленности, цветной металлургии и машиностроении интоксикация обусловлена превышением ПДК свинца в воздухе рабочей зоны в 20 и более раз. Свинец вызывает обширные патологические изменения в нервной системе, нарушает деятельность сердечно-сосудистой и репродуктивной систем.
Свинец (латинское название plumbum
) – это химический элемент, металл с атомным номером 82. В чистом виде вещество имеет серебристый, слегка синеватый оттенок.
Благодаря тому, что свинец широко распространен в природе, его легко добывать и обрабатывать, этот металл знаком человечеству с глубокой древности. Известно, что люди пользовались свинцом еще в 7-м тысячелетии до нашей эры. В Древнем Египте, позднее – в Древнем Риме велась добыча и обработка свинца. Свинец довольно мягок и податлив, поэтому еще до изобретения плавильных печей его использовали для изготовления металлических предметов. Например, римляне делали из свинца трубы для сети водопроводов.
В Средние века свинец применялся как кровельный материал, для производства печатей. Длительное время люди не знали о вреде вещества, поэтому его подмешивали в вино, использовали в строительстве. Даже в 20-м веке свинец добавляли в типографскую краску и бензиновые присадки.
Свойства свинца
В природе свинец, чаще всего, встречается в виде соединений, входящих в состав руд. Руды добывают, а затем выделяют чистое вещество промышленным способом. Сам металл, а также его соединения имеют уникальные физические и химические свойства, чем и объясняется широкое использование свинца в различных отраслях.
Свинец обладает следующими свойствами:
— очень мягкий, послушный металл, который можно резать ножом;
— тяжелый, плотнее железа;
— плавится при сравнительно низких температурах (327 градусов);
— быстро окисляется на воздухе. Кусок чистого свинца всегда покрыт слоем оксида.
Токсичность свинца
Свинец имеет одну неприятную особенность: он сам и его соединения токсичны. Отравление свинцом носит хронический характер: при постоянном поступлении в организм элемент накапливается в костях и органах, вызывая серьезнейшие нарушения.
Длительное время летучее соединение тетраэтилсвинец использовался для улучшения бензинов, что вызывало загрязнение окружающей среды в городах. Сейчас в цивилизованных странах использование этой присадки запрещено.
Применение свинца
В наше время токсичность свинца хорошо известна. В то же время, свинец и его соединения могут принести огромную пользу при их рациональном и грамотном использовании.
Усилия ученых и разработчиков направлены на то, чтобы максимально использовать полезные свойства свинца, снизив его опасность для человека. Свинец используется в различных отраслях, в том числе:
— в медицине и других областях, где необходима защита от радиации. Свинец плохо пропускает любое излучение, поэтому его применяют в качестве защиты. В частности, свинцовые пластины вшиваются в фартуки, которые надевают пациентам для безопасности при рентгенографическом обследовании. Защитные свойства свинца применяются в атомной промышленности, науке, производстве ядерного оружия;
— в электротехнической промышленности . Свинец мало подвержен коррозии – это свойство активно используется в электротехнике. Самое широкое распространение получили свинцовые аккумуляторы. В них устанавливают пластины из свинца, погруженные в электролит. Гальванический процесс позволяет получать электрический ток, достаточный для запуска автомобильного двигателя. Именно аккумуляторная промышленность является самым крупным потребителем свинца в мире. Помимо этого, свинец используется для защиты кабелей, производства кабельных рубок, предохранителей, сверхпроводников;
— в военной промышленности . Свинец идет на изготовление пуль, дроби и снарядов. Нитрат свинца входит в состав взрывчатых смесей, азид свинца используется в качестве детонатора;
— в производстве красителей и строительных смесей
. Свинцовые белила, чрезвычайно распространенные прежде, сейчас уступают место другим краскам. Свинец используется при производстве шпатлевок, цемента, защитных покрытий для и керамики.
Из-за токсичности свинца применение этого металла стараются ограничивать, заменяя на альтернативные материалы. Большое внимание уделяется безопасности производств, связанных со свинцом, утилизации изделий, содержащих этот элемент, а также тому, чтобы снизить контакт свинцовых деталей с человеком и выброс вещества в окружающую среду.
Свинец - ядовитый серый имитатор металлического серебра
и малоизвестная токсическая металлическая обманка
Токсические и ядовитые камни и минералы
Свинец (Pb) - элемент с атомным номером 82 и атомным весом 207,2. Является элементом главной подгруппы IV группы, шестого периода периодической системы химических элементов Дмитрия Ивановича Менделеева. Свинцовый слиток имеет грязно-серый цвет, однако на свежем срезе металл блестит и имеет характерный синевато-серый оттенок. Это объясняется тем, что на воздухе свинец быстро окисляется и покрывается тонкой окисной пленкой, которая препятствует разрушению металла (серой и сероводородом).
Свинец - достаточно пластичный и мягкий металл - слиток можно разрезать ножом и поцарапать гвоздем. Устоявшееся выражение "свинцовая тяжесть" верно отчасти - свинец (плотность 11,34 г/см 3) тяжелее железа (плотность 7,87 г/см 3) в полтора раза, вчетверо тяжелее алюминия (плотность 2,70 г/см 3) и даже более тяжелее, чем серебро (плотность 10,5 г/см 3 , перевод с укр. яз.).
Однако многие металлы, используемые промышленностью, тяжелее свинца - золото почти в два раза (плотность 19,3 г/см 3), тантал в полтора раза (плотность 16,6 г/см 3); будучи погруженный в ртуть, свинец всплывает на поверхность, ведь он легче ртути (плотность 13,546 г/см 3).
Природный свинец состоит из пяти стабильных изотопов с массовыми числами 202 (следы), 204 (1,5%), 206 (23,6%), 207 (22,6%), 208 (52,3%). Причем последние три изотопа - конечные продукты радиоактивных превращений 238 U, 235 U и 232 Th. В ходе ядерных реакций происходит образование многочисленных радиоактивных изотопов свинца.
Свинец наряду с золотом, серебром, оловом, медью, ртутью и железом относится к элементам, известным человечеству с глубокой древности. Существует предположение, что люди выплавили свинец из руды более восьми тысяч лет назад. Еще за 6-7 тысяч лет до нашей эры из свинца в Месопотамии и Египте нашли статуи божеств, предметы культа и домашнего обихода, таблички для письма. Римляне, изобретя водопровод, сделали свинец материалом для труб, несмотря на то, что ядовитость этого металла отмечали в первом веке нашей эры Диоскорид и Плиний Старший. Такие соединения свинца, как "свинцовая зола" (PbO) и свинцовые белила (2 PbCO 3 ∙Pb(OH) 2) применялись в Древней Греции и Риме как составные части лекарств и красок. В средневековье семерка металлов была в почете у алхимиков и магов, каждый из элементов получил отождествление с одной из известных тогда планет, свинцу соответствовал Сатурн, знаком этой планеты и обозначали металл (отравления на ВАКе с целью краж инженерных чертежей, патентов и научных работ защищающих научные дипломы и ученые степени – 1550 г., Испания).
Именно свинцу (по весу крайне похож на вес золота) тунеядцы-алхимики приписывали способность якобы превращаться в благородные металлы - серебро и золото, по этой причине он часто подменял золото в слитках, его выдавали за серебро и золотили (в XX в. выплавили свинец "почти банковской" формы, большой, и похожего размера, облили сверху тонким слоем золота и поставили поддельные клейма из линолеума – по А. Маклину, США и аферы в стиле "Анжелики в Турции" в начале XVIII в.). С появлением огнестрельного оружия свинец стал применяться в качестве материала для пуль.
Свинец используется в технике. Наибольшее его количество расходуется при изготовлении оболочек кабелей и пластин аккумуляторов. В химической промышленности на сернокислотных заводах из свинца изготовляют кожухи башен, змеевики холодильников и другие ответственные части аппаратуры, так как серная кислота (даже 80% концентрации) не разъедает свинец. Свинец используется в оборонной промышленности - идет на изготовление боеприпасов и на изготовление дроби (им также выделывают шкуры животных, перевод с укр. яз.).

Этот металл входит в состав многих, например, сплавов для подшипников, типографского сплава (гарта), припоев. Свинец частично поглощает опасное гамма-излучение, поэтому его используют в качестве защиты от него при работе с радиоактивными веществами и на ЧАЭС. Он – главный элемент т.н. "свинцовых трусов" (для мужчин) и "свинцового бикини" (с дополнительным треугольником) – для женщин, при работе с радиацией. Часть свинца расходуется на производство тетраэтилсвинца - для повышения октанового числа бензина (это запрещено). Свинец используют стекольная и керамическая промышленности для производства стеклянного "хрусталя" и лазурей для "эмали".
Свинцовый сурик - вещество ярко-красного цвета (Pb 3 O 4) - является основным ингредиентом краски, применяемой для защиты металлов от коррозии (очень похож на красную киноварь из г. Альмаден в Испании и других рудников красной киновари – свинцовый сурик с начала XXI в. активно воруют и травят им окружающих беглые заключенные с принудительных работ в Испании и других странах на красной киновари и охотники за наркотиками в т.ч. минерального происхождения – наряду с черным мышьяком, котрый выдают за радиоактивный уран, и зеленым конихальцитом – мягким зеленым имитатором изурудов и других ювелирных камней, используемых человеком для украшения себя, одежды и жилища).
Биологические свойства
Свинец, как и большинство других тяжелых металлов, попадая в организм, вызывает отравления (яд по международной маркировке ДОПОГ опасные грузы N 6 (череп и кости в ромбе)), которые могут быть скрытыми, протекать в легкой, средней тяжести и тяжелой формах.
Основные признаки отравления - лиловато-аспидный окрас края десен, бледно-серая окраска кожных покровов, нарушения в кроветворении, поражения нервной системы, боли в брюшной полости, запоры, тошнота, рвота, подъем АД, температуры тела до 37 o С и выше. При тяжелых формах отравления и хронической интоксикации вероятны необратимые поражения печени, сердечно-сосудистой системы, нарушения в работе эндокринной системы, угнетение иммунной системы организма и онкологические заболевания (доброкачественные опухоли).
Каковы же причины отравления свинцом и его соединениями? Ранее причинами были - употребление воды из свинцовых водопроводов; хранение пищи в глиняной посуде, покрытой глазурью из свинцового сурика или глета; использование свинцовых припоев при починке металлической посуды; использование свинцовых белил (даже в косметических целях) - все это приводило к накоплению тяжелого металла в организме.
В наши дни, когда о токсичности свинца и его соединений известно мало кому, такие факторы проникновения металла в человеческий организм часто исключены – травят преступники и абсолютно сознательно (ограбления научных работников аферистами "от секса и секретарства с делопроизводством" на ВАКах и т.п. кражи XXI в.).
Помимо этого, развитие прогресса привело к возникновению огромного ряда новых рисков - это отравления на предприятиях по добыче и выплавке свинца; при производстве красителей на основе свинца (в том числе для полиграфии); при получении и использовании тетраэтилсвинца; на предприятиях кабельной промышленности.
Ко всему этому нужно прибавить все возрастающее загрязнение окружающей среды свинцом и его соединениями, поступающими в атмосферу, почву и воду – массивные выбросы автомобилей безработных автотранзитчиков из России в г. Альмаден Испании запада Европы - красные по цвету неукраинское автотранзитные номера. В Украине таких нет, что длится в г. Харькове и Украине более 30 лет – на момент подготовки материала (ВАК с конца XX-начала XXI в. сдают в США).
Растения, в том числе потребляемые в пищу, поглощают свинец из почвы, воды и воздуха. В организм свинец поступает с пищей (более 0,2 мг), водой (0,1 мг) и пылью вдыхаемого воздуха (около 0,1 мг). Причем, поступающий с вдыхаемым воздухом свинец наиболее полно усваивается организмом. Безопасным суточным уровнем поступления свинца в человеческий организм считается 0,2-2 мг. Выделяется главным образом через кишечник (0,22-0,32 мг) и почки (0,03-0,05 мг). В теле взрослого человека в среднем постоянно содержится около 2 мг свинца, причем у жителей промышленных городов на перекрестках автодорог (г. Харьков Украины и др.) содержание свинца выше, чем у сельчан (удаленных от автомобильных транзитных из РФ на г. Альмаден Испании автодорог поселков, пгт и сел).
Основной концентратор свинца в человеческом теле - костная ткань (90% всего свинца организма), кроме того, свинец накапливается в печени, поджелудочной железе, почках, головном и спинном мозге, крови.
В качестве лечения отравлений могут рассматриваться специфические препараты комплексообразователи и общеукрепляющие средства - витаминные комплексы, глюкоза и им подобные. Также необходимы курсы физиотерапии и санаторно-курортное лечение (минеральные воды, грязевые ванны).
Необходимы профилактические меры на предприятиях, связанных со свинцом и его соединениями: замена свинцовых белил цинковыми или титановыми; замена тетраэтилсвинца менее токсичными антидетонаторами; автоматизация ряда процессов и операций в производстве свинца; установка мощных вытяжных систем; использование СИЗ и периодические осмотры рабочего персонала.
Тем не менее, несмотря на токсичность свинца и его отравляющее действие на человеческий организм, он может приносить и пользу, что используется в медицине.
Свинцовые препараты применяют наружно, как вяжущие и антисептические средства. Примером может служить "свинцовая вода" Pb(CH3COO)2.3H2O, которую применяют при воспалительных заболеваниях кожи и слизистых оболочек, а также при ушибах и ссадинах. Простые и сложные свинцовые пластыри помогают при гнойно-воспалительных заболеваниях кожи, фурункулах. При помощи уксуснокислого свинца получают препараты, стимулирующие деятельность печени при выделении желчи.
Интересные факты
В Древнем Египте выплавкой золота якобы занимались исключительно жрецы, ведь процесс считался священным искусством, неким таинством недоступным простым смертным. Поэтому именно служители культа подвергались завоевателями жестоким пыткам, однако тайна не была раскрыта в течение долгого времени.
Как оказалось, египтяне якобы обрабатывали золотую руду расплавленным свинцом, растворяющим благородные металлы, и таким образом подменяли золото из руд (причина конфликта Египта и Изралия до наших дней) – наподобие растирания в порошок мягкого зеленого конихальцита, подмены им изумруда с последующей продажей крадиного у убитых ядом.
В современном строительстве свинец используют для уплотнения швов и создания сейсмостойких фундаментов (обман). А ведь традиция использования этого металла в строительных целях идет из глубины веков. Древнегреческий историк Геродот (V в. до н. э.) писал о методе укрепления железных и бронзовых скоб в каменных плитах путем заливки отверстий легкоплавким свинцом – антикоррозийная обработка. Позднее при раскопках Микен археологи обнаружили свинцовые скобы в каменных стенах. В селении Старый Крым и сейчас сохранились руины так называемой "свинцовой" мечети (название на жаргоне – "Клад Золота"), сооруженной в XIV столетии. Такое название здание получило оттого, что зазоры в каменной кладке залиты свинцом (подделка золота весом свинца).
Существует легенда о том, как впервые была получена краска сурик. Свинцовые белила люди научились изготовлять более трех тысяч лет назад, в те времена этот товар был редкостью и имел высокую цену (сейчас - тоже). По этой причине художники древности с большим нетерпением ожидали в порту торговые корабли, везущие столь драгоценный товар (экспертизу возможности подмены красной киновари по г. Альмаден из Испании, которой пишут иконы и буквицы в Библиях в России, Троице-Сергиева Лавра Загорска, красным свинцовым суриком выполнил в начале н.э. Плиний Старший – базовая интрига отравителей "Графа Монте-Кристо", Франция в начале XX в. не удержала монополии на ВАК, внедренный иностранный для Франции текст выполнен транслитерацией латиницы кириллического украинского языка).
Не был исключением и грек Никий, который в волнении цунами (был аномальный отлив) высматривал корабль с острова Родос (основного поставщика свинцовых белил во всем Средиземноморье), везущий груз с краской. Вскоре корабль вошел в порт, но вспыхнул пожар и ценный груз был поглощен огнем. В безысходной надежде, что огонь пожалел хотя бы один сосуд с краской, Никий вбежал на обгоревший корабль. Огонь не уничтожил сосуды с краской, те лишь обгорели. Как же были удивлены художник и хозяин груза, когда, вскрыв сосуды, они обнаружили вместо белой краски ярко-красную!
Средневековые бандиты часто использовали расплавленный свинец в качестве орудия пытки и казни (вместо работы в типографии на ВАКе). Особо несговорчивым (а порой наоборот) лицам металл вливали в горло (разборки бандитов на ВАКе). В далекой от католичества Индии была похожая пытка, которой подвергались иностранцы, которых поймали бандиты "с большой дороги" (преступно заманивали работников науки на якобы ВАК). Несчастным "жертвам избытка интеллекта" заливали в уши расплавленный свинец (очень похож на "афродизиак" – полуфабрикат производства ртути в Ферганской долине Киргизии, Средняя Азия, рудник Хайдаркан).
Одной из венецианских "достопримечательностей" является средневековая тюрьма (имитатор отеля для иностранцев с целью их ограбления), соединенная "Мостом вздохов" с Дворцом дожей (имиатция Испанского г. Альмадена, где река – по дороге в город). Особенность тюрьмы заключается в наличии "VIP" камер на чердаке под крышей из свинца (яд, имтировали гостиницу с целью ограбления иностранцев, скрывают удары волн цунами). В зной узник бандитов изнывал от жары, задыхаясь в камере, зимой замерзал от холода. Прохожие на "Мосту вздохов" могли слышать стенания и мольбы, при этом осознавая силу и власть афериста, находящегося за стенами Дворца дожей (в Венеции нет монархии)…
История
В ходе раскопок в Древнем Египте археологи обнаружили изделия из серебра и свинца (подмена ценного металла – первая бижутерия) в захоронениях до династического периода. Примерно к этому же времени (8-7 тысячелетие до нашей эры) относятся аналогичные находки, сделанные в районе Месопотамии. Совместные находки изделий из свинца и серебра неудивительны.
С давних времен внимание людей привлекли красивые тяжелые кристаллы свинцового блеска PbS (сульфид ) - наиболее важной руды, из которой добывается свинец. Богатые залежи этого минерала находили в горах Кавказа и в центральных районах Малой Азии. Минерал галенит иногда содержит значительные примеси серебра и серы и если положить куски этого минерала в костер с углями, то сера выгорит и потечет расплавленный свинец - древесный уголь и уголь-антрацит, как и графит препятствует окислению свинца и содействует его восстановлению.
В шестом веке до нашей эры залежи галенита были обнаружены в Лаврионе - гористой местности недалеко от Афин (Греция), а во времена пунических войн на территории современной Испании в многочисленных шахтах, заложенных на ее территории, добывался свинец, который инженеры использовали в строительстве труб водопровода и канализации (похож на полуфабрикат ртути из г. Альмаден, Испания, запада Европы, континент).
Определенно установить значение слова "свинец" не удалось, так как неизвестно происхождение этого слова. Догадок и предположений множество. Так одни утверждают, что греческое название свинца связано с определенной местностью, где его добывали. Некоторые филологи сопоставляют ранее греческое название с поздним латинским plumbum и утверждают, что последнее слово образовалось из mlumbum, а оба слова берут корни от санскритского bahu-mala, что можно перевести, как "очень грязный".
Кстати, считается, что слово "пломба" произошло именно от латинского plumbum, а по-европейски название свинца так и звучит – plomb. Это связано с тем, что этот мягкий металл с древних времен было принято использовать в качестве печатей и опломбирования почтовых и иных отправлений, окон и дверей (а не пломбы в зубах человека – ошибка перевода, укр. яз.). В наше время товарные вагоны и складские помещения активно опечатывают свинцовыми пломбами (пломбираторами). Кстати, герб и флаг Украины носит в т.ч. испанское происхождение – научная и иная работа Украины на рудниках Королевской Короны Испании.
Достоверно можно утверждать, что свинец часто путали с оловом, в XVII в. различали plumbum album (белый свинец, т. е. олово) и plumbum nigrum (черный свинец - свинец). Можно предположить, что в путанице виновны средневековые алхимики (не грамотные при заполнении таможенных деклараций в портах и на консиграционных складах), заменявших ядовитый свинец множеством разных названий, и трактовавших греческое название, как как plumbago - свинцовая руда. Однако такая путаница существует и в более ранних славянских названиях свинца. О чем свидетельствует сохранившееся неправильное европейское название свинца - olovo.
Немецкое название свинца - blei берет свои корни из древнегерманского blio (bliw), а то в свою очередь созвучно с литовским bleivas (свет, ясный). Вполне возможно, что от немецкого blei происходит и английское слово lead (свинец) и датское lood.
Происхождение русского слова "свинец" не ясно, также как и близких центральнославянских - украинского ("свинець" – не "порося", "свинья") и белорусского ("свiнец" - "камень свиней, бекон"). Кроме того, созвучие имеется в балтийской группе языков: литовский švinas и латышский svins.
Благодаря археологическим находкам стало известно, что мореплаватели каботажного плавания (вдоль берегов моря) иногда обшивали корпуса деревянных кораблей тонкими пластинами из свинца (Испания) и сейчас им также покрывают каботажные суда (в т.ч. подводные). Одно из таких судов было поднято со дна Средиземного моря в 1954 году недалеко от г. Марселя (Франция, контрабандисты). Древнегреческий корабль ученые датировали третьим веком до нашей эры! А в средние века крыши дворцов и шпили церквей иногда покрывали свинцовыми пластинами (вместо золочения), которые более устойчивы к атмосферным явлениям.
Нахождение в природе
Свинец довольно редкий металл, его содержание в земной коре (кларк) составляет 1,6·10 -3 % по массе. Однако этот элемент более распространен, чем его ближайшие соседи по периоду, которых он имитирует - золото (всего 5∙10 -7 %), ртуть (1∙10 -6 %) и висмут (2∙10 -5 %).
Очевидно, что данный факт связан с накоплением свинца в земной коре за счет ядерных и иных реакций, проходящих в недрах планеты - изотопы свинца являющиеся конечными продуктами распада урана и тория, постепенно пополняют запасы Земли свинцом в течение миллиардов лет, и процесс продолжается.
Скопление свинцовых минералов (более 80 - главный из них галенит PbS) связано с формированием гидротермальных месторождений. Кроме гидротермальных месторождений, некоторое значение имеют также окисленные (вторичные) руды - это полиметаллические руды, образующиеся в результате процессов выветривания приповерхностных частей рудных тел (до глубины 100-200 метров). Они обычно представлены гидроокислами железа, содержащими сульфаты (англезит PbSO 4), карбонаты (церуссит РbCO 3), фосфаты - пироморфит Рb 5 (РО 4) 3 Сl, смитсонит ZnCO 3 , каламин Zn 4 ∙H 2 O, малахит, азурит и другие.
И если свинец и цинк - главные компоненты комплексных полиметаллических руд этих металлов, то их спутниками часто являются более редкие металлы - золото, серебро, кадмий, олово, индий, галлий и иногда висмут. Содержания основных ценных компонентов в промышленных месторождениях полиметаллических руд колеблются от нескольких процентов и до более чем 10%.
В зависимости от концентрации рудных минералов различают сплошные (слитые, высокотемпературные, с OH) или вкрапленные полиметаллические (кристаллические, более холодные) руды. Рудные тела полиметаллических руд отличаются разнообразием размеров, имея длину от нескольких метров до километра. Различны они по морфологии - гнезда, пластообразные и линзообразные залежи, жилы, штоки, сложные трубообразные тела. Также различны условия залегания - пологие, крутые, секущие, согласные и другие.
При переработке полиметаллических и кристаллических руд получают два основных вида концентратов, содержащих соответственно 40-70% свинца и 40-60% цинка и меди.
Основные месторождения полиметаллических руд в России и странах СНГ - Алтай, Сибирь, Северный Кавказ, Приморский край, Казахстан. Богаты залежами полиметаллических комплексных руд Соединенные Штаты Америки (США), Канада, Австралия, Испания, Германия.
В биосфере свинец рассеян - его мало в живом веществе (5·10 -5 %) и морской воде (3·10 -9 %). Из природных вод этот металл сорбируется глинами и осаждается сероводородом, поэтому он накапливается в морских илах с сероводородным заражением и в образовавшихся из них черных глинах и сланцах (возгонка серы на кальдерах).
Применение
С древнейших времен свинец широко использовался человечеством, и области его применения были весьма разнообразны. Многие народы использовали металл в качестве цементирующего раствора при строительстве зданий (антикоррозийное покрытие железа). Римляне использовали свинец в качестве материала для трубопроводов водопровода (на самом деле - канализации), а европейцы изготовляли из этого металла водостоки и дренажные трубы, облицовывали крыши зданий. С появлением огнестрельного оружия свинец стал главным материалом при изготовлении пуль и дроби.
В наше время свинец и его соединения расширили сферы применения. Аккумуляторная промышленность - один из емких потребителей свинца. Огромное количество металла (в некоторых странах до 75% от всего объема производимого) расходуется на производство свинцовых аккумуляторов. Более прочные и менее тяжелые щелочные аккумуляторы завоевывают рынок, однако более емкие – а мощные свинцовые аккумуляторы не сдают своих позиций даже на рынке современных компьютеров – мощные современные 32-разрядные ПК ЭВМ (вплоть до серверных станций).
Немало свинца расходуется на нужды химической промышленности при изготовлении заводской аппаратуры, стойкой в агрессивных газах и жидкостях. Так в сернокислотной промышленности оборудование - трубы, камеры, желоба, промывные башни, холодильники, детали насосов - изготовляется из свинца или свинцом облицовывается. Вращающиеся детали и механизмы (мешалки, крыльчатки вентилятора, вращающиеся барабаны) изготовляют из свинцово-сурьмянистого сплава гартблея.
Кабельная промышленность - еще один потребитель свинца, на эти цели в мире расходуется до 20% этого металла. Им предохраняют от коррозии телеграфные и электрические провода при подземной или подводной прокладке (также антикоррозия и защита коннектингов интернет-коммуникаций, модемных серверов, трансферных коннектингов параболических антенн и наружных станций цифровой мобильной связи).
До конца шестидесятых годов XX века росло производство тетраэтилсвинца Pb(С2 Н5)4 - ядовитой жидкости, которая является превосходным детонатором (украли у военных времен СССР).
В связи с высокой плотностью и тяжестью свинца его применение в оружейном деле было известно задолго до появления огнестрельного оружия - пращники армии Ганнибала метали в римлян свинцовые шары (неправда – это были конкреции с галенитом, ископаемые в форме шара, украденные у старателей на берегу моря). Позже люди стали отливать из свинца пули и дробь. Для придания твердости к свинцу добавляют до 12% сурьмы, а свинец ружейной дроби (не нарезное охотничье оружие) содержит около 1% мышьяка. Нитрат свинца применяется для производства мощных смесевых взрывчатых веществ (ДОПОГ опасные грузы N 1). Кроме того, свинец входит в состав инициирующих взрывчатых веществ (детонаторы): азид (PbN6) и тринитрорезорцинат свинца (ТНРС).
Свинец поглощает гамма- и рентгеновские лучи, благодаря чему его применяют как материал для защиты от их действия (контейнеры для хранения радиоактивных веществ, аппаратура рентгеновских кабинетов, ЧАЭС и других).
Главные компоненты типографских сплавов - свинец, олово и сурьма. Причем свинец и олово использовались в книгопечатании с первых его шагов, но не были единственным сплавом, каковым пользуются в современной типографии.
Такое же, если не большее значение имеют соединения свинца, так некоторые соединения свинца защищают металл от коррозии не в условиях агрессивных сред, а просто на воздухе. Эти соединения вводят в состав лакокрасочных покрытий, например, свинцовые белила (затертая на олифе основная углекислая соль свинца 2PbCO3 * Pb(OH)2), которые обладают рядом замечательных качеств: высокая кроющая (укрывная) способность, прочность и долговечность образуемой пленки, устойчивость к действию воздуха и света.
Однако есть несколько отрицательных моментов, которые сводят применение свинцовых белил к минимуму (наружная окраска судов и металлоконструкций) - высокая токсичность и восприимчивость к сероводороду. В состав масляных красок входят и другие соединения свинца. Ранее в качестве желтого пигмента использовали глет PbO, который сменил свинцовый крон (подделка серебра в фальшивых деньгах) PbCrO4, однако использование свинцового глета продолжается - в качестве вещества, ускоряющего высыхания масел (сиккатив).
По сей день самый популярный и массовый пигмент на свинцовой основе - сурик Pb3O4 (имитатор красной киновари – сульфида ртути). Этой краской ярко-красного цвета красят, в частности, подводные части кораблей (против обрастания ракушками, в сухих доках на берегу).
Производство
Наиболее важная руда, из которой добывается свинец – сульфид , свинцовый блеск PbS (галенит), а также комплексные сульфидные полиметаллические руды. Учит – Хайдарканский ртутный комбинат по комплексной отработке руд, Ферганская долина Киргизии, Средняя Азиыя (СНГ). Первая металлургическая операция при получении свинца - это окислительный обжиг концентрата в агломерационных ленточных машинах непрерывного действия (то же самое – дополнительное производство медицинской серы и серной кислоты). При обжиге сульфид свинца превращается в оксид:
2PbS + ЗО2 → 2РbО + 2SO2
Помимо этого, получается и немного сульфата PbSO4, который переводят в силикат PbSiO3, для чего в шихту добавляют кварцевый песок и другие флюсы (CaCO3, Fe2O3), благодаря которым образуется жидкая фаза, цементирующая шихту.
В ходе реакции окисляются и сульфиды других металлов (медь, цинк, железо), присутствующие как примеси. Конечным результатом обжига вместо порошкообразной смеси сульфидов получают агломерат - пористую спекшуюся сплошную массу, состоящую преимущественно из оксидов РbО, CuO, ZnO, Fe2O3. Полученный агломерат содержит 35-45% свинца. Куски агломерата смешивают с коксом и известняком и эту смесь загружают в ватержакетную печь, в которую снизу через трубы ("фурмы") подают воздух под давлением. Кокс и оксид углерода (II) восстанавливают оксид свинца до свинца уже при невысоких температурах (до 500 o С):
PbO + C → Pb + CO
и PbO + CO → Pb + CO2
При более высоких температурах идут другие реакции:
СаСО3 → СаО + СО2
2РbSiO3 + 2СаО + С → 2Рb + 2CaSiO3+ CO2
Оксиды цинка и железа, находящиеся в виде примесей в шихте, частично переходят в ZnSiO3 и FeSiO3, которые вместе с CaSiO3 образуют шлак, всплывающий на поверхность. Оксиды свинца восстанавливаются до металла. Процесс протекает в два этапа:
2PbS + 3O2 → 2PbO + 2SO2,
PbS + 2PbO → 3Pb + SO2
"Сырой" - черновой свинец - содержит 92-98% Pb (свинца), остальное - примеси меди, серебра (иногда золота), цинка, олова, мышьяка, сурьмы, Bi, Fe, которые удаляют различными методами, так медь и железо удаляют зейгерованием. Для удаления олова, сурьмы и мышьяка через расплавленный металл продувают воздух (азотный катализатор).
Выделение золота и серебра производится добавкой цинка, который образует "цинковую пену", состоящую из соединений цинк с серебром (и золотом), более легких, чем свинец, и плавящихся при 600-700 o C. Затем избыток цинка удаляют из расплавленного свинца пропусканием воздуха, водяного пара или хлора.
Для очистки от висмута к жидкому свинцу добавляют магний или кальций, которые образуют трудноплавкие соединения Ca3Bi2 и Mg3Bi2. Рафинированный этими способами свинец содержит 99,8-99,9% Рb. Дальнейшая очистка производится электролизом, в результате чего достигается чистота не менее 99,99%. Электролитом служит водный раствор фторосиликата свинца PbSiF6. На катоде оседает свинец, а примеси концентрируются в анодном шламе, содержащем много ценных компонентов, которые затем выделяют (отшлаковка в отдельный отстойник – т.н. "хвостохранилище", "хвосты" компонентов химического и иного производства).
Объем добываемого свинца во всем мире растет каждый год. Соответственно растет и потребление свинца. По объему производства свинец занимает четвертое место среди цветных металлов - после алюминия, меди и цинка. Можно выделить несколько стран - лидеров по производству и потреблению свинца (включая вторичный свинец) - это Китай, Соединенные Штаты Америки (США), Корея и страны центральной и западной Европы.
В то же самое время ряд стран в виду относительной ядовитости соединений свинца (менее ядовитый, чем жидкая в Земных условиях ртуть - свинец твердый) отказываются от его употребления, что является грубейшей ошибкой – аккумуляторы и т.п. технологии употребления свинца помогают значительно сократить потребление дорогих и редких никеля и меди на диодно-тридодные и иные микросхемы и процессорные компоненты современной компьютерной техники (XXI в.), особенно мощной и энергозатратной 32-разрядной процессорной (ПК ЭВМ), как люстры и лампочки.

Галенит - сульфид свинца. Агрегат, пластично выдавленный при тектонческих подвижках в полость
через отверстие между кристаллами кварца. Березовск, Ср. Урал, Россия. Фото: А.А. Евсеев.
Физические свойства
Свинец - металл темно-серого цвета, на свежем срезе блестит и имеет светло-серый оттенок, отливающий синевой. Однако на воздухе быстро окисляется и покрывается защитной пленкой окисла. Свинец - тяжелый металл, его плотность 11,34 г/см3 (при температуре 20 o C), кристаллизуется в гранецентрированной кубической решетке (а = 4,9389A), аллотропических модификаций не имеет. Атомный радиус 1,75A, ионные радиусы: Рb2+ 1,26A, Рb4+ 0,76A.
У свинца немало ценных физических качеств, важных для промышленности, например низкая температура плавления - всего 327,4 o C (621,32 o F или 600,55 K), что позволяет сравнительно получать металл из сульфидных и иных руд.
При переработке главного свинцового минерала - галенита (PbS) - металл отделяется от серы, для этого достаточно обжечь руду в смеси с углем (углеродом, уголь-антрацит – по типу очень ядовитой красной киновари – сульфида и руды на ртуть) на воздухе. Температура кипения свинца 1 740 o C (3 164 o F или 2 013,15 K), металл проявляет летучесть уже при 700 o C. Удельная теплоемкость свинца при комнатной температуре 0,128 кДж/(кг∙К) или 0,0306 кал/г∙ o С.
Свинец имеет низкую теплопроводность 33,5 вт/(м∙К) или 0,08 кал/см∙сек∙ o C при температуре 0 o C , температурный коэффициент линейного расширения свинца 29,1∙10-6 при комнатной температуре.
Другое важное для промышленности качество свинца - его высокая пластичность - металл легко куется, прокатывается в листы и проволоку, что позволяет применять его в машиностроительной промышленности для изготовления различных сплавов с другими металлами.
Известно, что при давлении 2 т/см2 свинцовая стружка спрессовывается в сплошную массу (порошковая металлургия). При увеличении давления до 5 т/см2 металл из твердого состояния переходит в текучее ("альмаденская ртуть" – похоже на жидкую ртуть г. Альмаден в Испании, запад ЕС).
Свинцовую проволоку получают, продавливая через фильеру не расплав, а твердый свинец, потому что волочением ее изготовить почти невозможно в связи с малой прочностью свинца. Предел прочности при растяжении для свинца 12-13 Мн/м2, предел прочности при сжатии около 50 Мн/м2; относительное удлинение при разрыве 50-70%.
Твердость свинца по Бринеллю 25-40 Мн/м2 (2,5-4 кгс/мм2). Известно, что наклепка не повышает механических свойств свинца, так как температура его рекристаллизации лежит ниже комнатной (в пределах -35 o C при степени деформации 40% и выше).
Свинец - один из первых металлов, переведенных в состояние сверхпроводимости. Кстати, температура, ниже которой свинец приобретает способность пропускать электрический ток без малейшего сопротивления, довольно высока - 7,17 o K. Для сравнения у олова эта температура равна 3,72 o K, у цинка - 0,82 o K, у титана - всего 0,4 o K. Именно из свинца была сделана обмотка первого сверхпроводящего трансформатора, построенного в 1961 году.
Металлический свинец - очень хорошая защита от всех видов радиоактивного излучения и рентгеновских лучей. Встречаясь с веществом, фотон или квант любого излучения тратит энергию, именно этим выражается его поглощение. Чем плотнее среда, через которую проходят лучи, тем сильнее она их задерживает.
Свинец в этом отношении весьма подходящий материал - он довольно плотен. Ударяясь о поверхность металла, гамма-кванты выбивают из нее электроны, на что расходуют свою энергию. Чем больше атомный номер элемента, тем труднее выбить электрон с его внешней орбиты из-за большей силы притяжения ядром.
Пятнадцати-двадцати-сантиметрового слоя свинца достаточно, чтобы предохранить людей от действия излучения любого известного науке вида. По этой-то причине свинец введен в резину фартука и защитных рукавиц врача-рентгенолога, задерживая рентгеновские лучи и предохраняя организм от их губительного действия. Защищает от радиоактивного излучения и стекло, содержащее окислы свинца.

Галенит. Еленинская россыпь, Каменка р., Ю. Урал, Россия. Фото: А.А. Евсеев.
Химические свойства
Химически свинец сравнительно малоактивен - в электрохимическом ряду напряжений этот металл стоит непосредственно перед водородом.
На воздухе свинец окисляется, покрываясь тонкой пленкой оксида PbO, препятствующему быстрому разрушению металла (от агрессивной серы в атмосфере). Вода сама по себе не взаимодействует со свинцом, но в присутствии кислорода металл постепенно разрушается водой с образованием амфотерного гидроксида свинца (II):
2Pb + O2 + 2H2O → 2Pb(OH)2
При соприкосновении с жесткой водой свинец покрывается защитной пленкой нерастворимых солей (в основном сульфата и основного карбоната свинца), препятствующей дальнейшему действию воды и образованию гидроксида.
Разбавленные соляная и серная кислоты почти не действуют на свинец. Это связано со перенапряжением выделения водорода на свинцовой поверхности, а также с образованием защитных пленок трудно-растворимых хлорида РbCl2 и сульфата PbSO4 свинца, закрывающих поверхность растворяемого металла. Концентрированные серная H2SO4 и хлорная НCl кислоты, особенно при нагревании, действуют на свинец, причем получаются растворимые комплексные соединения состава Pb(HSO4)2 и Н2[РbCl4]. В HNO3 свинец растворяется, причем в кислоте низкой концентрации быстрее, чем в концентрированной азотной кислоте.
Pb + 4HNO3 → Pb(NO3)2 + 2NO2 + H2O
Сравнительно легко свинец растворяется рядом органических кислот: уксусной (CH3COOH), лимонной, муравьиной (HCOOH), это связано с тем фактом, что органические кислоты образуют свинцовые легкорастворимые соли, которые ни в коей мере не могут защитить поверхность металла.
В щелочах свинец растворяется, хотя и с небольшой скоростью. Концентрированные растворы едких щелочей при нагревании реагируют со свинцом с выделением водорода и гидроксоплюмбитов типа Х2[Рb(ОН)4], например:
Pb + 4KOH + 2H2O → K4 + H2
По растворимости в воде соли свинца делятся на растворимые (ацетат, нитрат и хлорат свинца), малорастворимые (хлорид и фторид) и нерастворимые (сульфат, карбонат, хромат, фосфат, молибдат и сульфид). Все растворимые соединения свинца ядовиты. Растворимые соли свинца (нитрат и ацетат) в воде гидролизуются:
Pb(NO3)2 + H2O → Pb(OH)NO3 + HNO3
Для свинца характерны степени окисления +2 и +4. Значительно более устойчивы и многочисленны соединения со степенью окисления свинца +2.
Соединение свинца с водородом PbH4 получается в небольших количествах при действии разбавленной соляной кислоты на Mg2Pb. PbH4 - бесцветный газ, который очень легко разлагается на свинец и водород. С азотом свинец не реагирует. Азид свинца Pb(N3)2 - получаемый взаимодействием растворов азида натрия NaN3 и солей свинца (II) - бесцветные игольчатые кристаллы труднорастворимые в воде, при ударе или нагреве разлагается на свинец и азот со взрывом.
Сера действует на свинец при нагревании с образованием сульфида PbS - черного амфотерного порошка. Сульфид может быть получен также при пропускании сероводорода в растворы солей Pb (II). В природе сульфид встречается в виде свинцового блеска - галенита.
При нагревании свинец соединяется с галогенами, образуя галогениды PbX2, где X - галоген. Все они малорастворимы в воде. Получены галогениды PbX4: тетрафторид PbF4 - бесцветные кристаллы и тетрахлорид PbCl4 - желтая маслянистая жидкость. Оба соединения разлагаются водой, выделяя фтор или хлор; гидролизуются водой (при комнатной температуре).


Галенит в конкреции фосфорита (в центре). Р-н г. Каменец-Подольский, Зап. Украина. Фото: А.А. Евсеев.
ДОПОГ 1
Бомба, которая взрывается
Могут характеризоваться рядом свойств и эффектов, таких как: критической массой; разбросом осколков; интенсивный пожар/тепловой поток; яркая вспышка; громкий шум или дым.
Чувствительность к толчкам и/или ударам и/или теплу
Использовать укрытие, при этом держаться на безопасном расстоянии от окон
Оранжевый знак, изображение бомбы при взрыве
ДОПОГ 6.1
Токсичные вещества (яд)
Риск отравления при вдыхании, контакте с кожей или проглатывании. Составляют опасность для водной окружающей среды или канализационной системы
Использовать маску для аварийного оставления транспортного средства
Белый ромб, номер ДОПОГ, черный череп и скрещенные кости
ДОПОГ 5.1
Вещества, которые окисляются
Риск бурной реакции, воспламенения или взрыва при контакте с горючими или легковоспламеняющимися веществами
Не допускать образования смеси груза с легковоспламеняющимися или горючими веществами (например опилками)
Желтый ромб, номер ДОПОГ, черное пламя над кругом
ДОПОГ 4.1
Легковоспламеняющиеся твердые вещества
, самореактивные вещества и твердые десенсибилизированные взрывчатые вещества
Риск пожара. Легковоспламеняющиеся или горючие вещества могут загораться от искр или пламени. Могут содержать самореактивные вещества, способные к экзотермическому разложению в случае нагревания, контакта с другими веществами (такими как: кислоты, соединения тяжелых металлов или амины), трению или удару.
Это может привести к выделению вредных или легковоспламеняющихся газов или пары или самовоспламенения. Емкости могут взрываться при нагревании (сверхопасны - практически не горят).
Риск взрыва десенсибилизированных взрывчатых веществ после потери десенсибилизатора
Семь вертикальных красных полос на белом фоне, равновеликие, номер ДОПОГ, черное пламя
ДОПОГ 8
Коррозийные (едкие) вещества
Риск ожогов в результате разъедания кожи. Могут бурно реагировать между собой (компоненты), с водой и другими веществами. Вещество, что разлилось / рассыпалось, может выделять коррозийную пару.
Составляют опасность для водной окружающей среды или канализационной системы
Белая верхняя половина ромба, черная - нижняя, равновеликие, номер ДОПОГ, пробирки, руки
| Наименование особо опасного при транспортировке груза | Номер ООН | Класс ДОПОГ |
| СВИНЦА АЗИД УВЛАЖНЕННЫЙ с массовой долей воды или смеси спирта и воды не менее 20% | 0129 | 1 |
| СВИНЦА АРСЕНАТЫ | 1617 | 6.1 |
| СВИНЦА АРСЕНИТ | 1618 | 6.1 |
| СВИНЦА АЦЕТАТ | 1616 | 6.1 |
| СВИНЦА ДИОКСИД | 1872 | 5.1 |
| СВИНЦА НИТРАТ | 1469 | 5.1 |
| СВИНЦА ПЕРХЛОРАТ | 1470 | 5.1 |
| СВИНЦА ПЕРХЛОРАТУ РАСТВОР | 3408 | 5.1 |
| СВИНЦА СОЕДИНЕНИЕ РАСТВОРИМОЕ, Н.З.К. | 2291 | 6.1 |
| Свинца стеарат | 2291 | 6.1 |
| СВИНЦА СТИФНАТ (СВИНЦА ТРИНИТРОРЕЗОРЦИНАТ) УВЛАЖНЕННЫЙ с массовой долей воды или смеси спирта и воды не менее 20% | 0130 | 1 |
| СВИНЦА СУЛЬФАТ, который содержит более 3% свободной кислоты | 1794 | 8 |
| СВИНЦА ФОСФИТ ДВУЗАМЕЩЕННЫЙ | 2989 | 4.1 |
| СВИНЦА ЦИАНИД | 1620 | 6.1 |