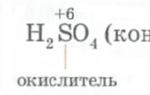Соединения азота. Свойства азота
АЗОТ, N (лат. Nitrogenium * а. nitrogen; н. Stickstoff; ф. azote, nitrogene; и. nitrogeno), — химический элемент V группы периодической системы Менделеева, атомный номер 7, атомная масса 14,0067. Открыт в 1772 английским исследователем Д. Резерфордом.
Свойства азота
При обычных условиях азот — газ без цвета и запаха. Природный азот состоит из двух стабильных изотопов: 14 N (99,635%) и 15 N (0,365%). Молекула азота двухатомная; атомы связаны ковалентной тройной связью NN. Диаметр молекулы азота, определённый разными способами, 3,15-3,53 А. Молекула азота очень устойчива — энергия диссоциации 942,9 кДж/моль.
Молекулярный азот
Константы молекулярного азота: f плавления — 209,86°С, f кипения — 195,8°С; плотность газообразного азота 1,25 кг/ м 3 , жидкого — 808 кг/м 3 .
Характеристика азота
В твёрдом состоянии азот существует в двух модификациях: кубической а-форме с плотностью 1026,5 кг/м 3 и гексагональной b-форме с плотностью 879,2 кг/м 3 . Теплота плавления 25,5 кДж/кг, теплота испарения 200 кДж/кг. Поверхностное натяжение жидкого азота в контакте с воздухом 8,5.10 -3 Н/м; диэлектрическая проницаемость 1,000538. Растворимость азота в воде (см 3 на 100 мл Н 2 О): 2,33 (0°С), 1,42 (25°С) и 1,32 (60°С). Внешняя электронная оболочка атома азота состоит из 5 электронов. Степени окисления азота меняются от 5 (в N 2 О 5) до -3 (в NH 3).
Соединение азота
Азот при нормальных условиях может реагировать с соединениями переходных металлов (Ti, V, Mo и др.), образуя комплексы либо восстанавливаясь с образованием аммиака и гидразина. С такими активными металлами, как , азот взаимодействует при нагревании до сравнительно невысоких температур. С большинством других элементов азот реагирует при высокой температуре и в присутствии катализаторов. Хорошо изучены соединения азота с : N 2 О, NO, N 2 О 5 . С азот соединяется только при высокой температуре и в присутствии катализаторов; при этом образуется аммиак NH 3 . С галогенами азот непосредственно не взаимодействует; поэтому все галогениды азота получают только косвенным путём, например фтористый азот NF 3 — при взаимодействии с аммиаком. С серой также не происходит непосредственного соединения азота. При взаимодействии раскалённого с азотом образуется циан (CN) 2 . При действии на обычный азот электрических разрядов, а также при электрических разрядах в воздухе может образоваться активный азот, представляющий собой смесь молекул и атомов азота, обладающих повышенным запасом энергии. Активный азот весьма энергично взаимодействует с кислородом, водородом, парами , и некоторыми металлами.
Азот — один из самых распространённых элементов на Земле, причём основная его масса (около 4.10 15 т) сосредоточена в свободном состоянии в . Ежегодно при вулканической деятельности в атмосферу выделяется 2.10 6 т азота. Незначительная часть азота концентрируется в (среднее содержание в литосфере 1,9.10 -3 %). Природные соединения азота — хлористый аммоний и различные нитраты (селитры). Нитриды азота могут образовываться только при высоких температурах и давлениях, что, по-видимому, имело место на самых ранних стадиях развития Земли. Крупные скопления селитры встречаются только в условиях сухого пустынного климата ( , и др.). Небольшие количества связанного азота находятся в (1-2,5%) и (0,02-1,5%), а также в водах рек, морей и океанов. Азот накапливается в почвах (0,1 %) и живых организмах (0,3%). Азот входит в состав белковых молекул и многих естественных органических соединений.
Круговорот азота в природе
В природе осуществляется круговорот азота, который включает цикл молекулярного атмосферного азота в биосфере, цикл в атмосфере химически связанного азота, круговорот захоронённого с органическим веществом поверхностного азота в литосфере с возвратом его обратно в атмосферу. Азот для промышленности ранее добывался целиком из месторождений природных селитр, число которых в мире весьма ограничено. Особенно крупные залежи азота в виде азотнокислого натрия находятся в Чили; добыча селитры в отдельные годы составляла более 3 млн. т.
Азот (N 2) был открыт Дж. Пристли в 1774 г. Название "азот" в переводе с греческого означает "безжизненный". Оно обусловлено тем, что азот не поддерживает процессы горения и дыхания. Но для всех основных процессов жизнедеятельности растительных и живых оргнизмов азот крайне важен.
Характеристика элемента
7 N 1s 2 2s 2 2p 3
Изотопы: 14 N (99,635%); 15 N (0,365%)
Кларк в земной коре 0,01 % по массе. В атмосфере 78,09 % по объему (75,6 % по массе). Азот входит в состав живой материи (белки, нуклеиновые кислоты и др. ОВ). В гидросфере азот присутствует в виде нитратов (NО 3). Атомы азота занимают 5-е место по распространенности во Вселенной.
Важнейшие N-содержащие неорганические вещества.
Свободный (молекулярный) азот
Атомы азота связаны между собой тремя ковалентными неполярными связями: одна из них - сигма-связь, 2 - пи-связи. Энергия разрыва связи очень велика
Физические свойства
При обычной температуре и атмосферном давлении N 2 - бесцветный газ, без запаха и вкуса, немного легче воздуха, очень плохо растворяется в воде. В жидкое состояние переводится с большим трудом (Ткип -196"С). Жидкий азот имеет большую теплоту испарения и применяется для создания низких температур (хладагент).
Способы получения
Азот присутствует в воздухе в свободном состоянии, поэтому промышленный способ получения заключается в разделении воздушной смеси (ректификация жидкого воздуха).
В лабораторных условиях небольшие количества азота можно получить следующими способами:
1. Пропускание воздуха над раскаленной медью, которая поглощает кислород за счет реакции: 2Cu + О 2 = 2СиО. Остается азот с примесями инертных газов.
2. Окислительно-восстановительное разложение некоторых солей аммония:
NH 4 NО 2 = N 2 + 2Н 2 О
(NH 4) 2 Cr 2 О 7 = N 2 + Cr 2 О 3 + 4Н 2 О
3. Окисление аммиака и солей аммония:
4NH 3 + 3О 2 = 2N 2 + 6Н 2 О
8NH 3 + ЗВr 2 = N 2 + 6NH 4 Br
NH 4 Cl + NaNO 2 = N 2 + NaCl + 2Н 2 О
Химические свойства
Молекулярный азот - химически инертное вещество вследствие исключительно высокой устойчивости молекул N 2 . Только реакции соединения с металлами протекают более или менее легко. Во всех остальных случаях для инициирования и ускорения реакций необходимо применять высокие температуры, искровые электрические разряды, ионизирующее излучение, катализаторы (Fe, Cr, V, Ti и их соединения).
Реакции с восстановителями (N 2 - окислитель)
1. Взаимодействие с металлами:
Реакции образования нитридов щелочных и щелочноземельных Me протекают как с чистым азотом, так и при горении металлов на воздухе
N 2 + 6Li = 2Li 3 N
N 2 + 6Cs = 2Cs 3 N
N 2 + 3Mg = Mg 3 N 2
2. Взаимодействие с водородом (реакция имеет большое практическое значение):
N 2 + ЗН 2 = 2NH 3 аммиак
3. Взаимодействие с кремнием и углеродом
2N 2 + 3Si = Si 3 N 4 нитрид кремния (IV)
N 2 + 2C = (CN) 2 дициан
2N 2 + 5C + 2Na 2 CО 3 = 4NaCN + 3CО 2 цианид натрия
Реакции с окислителями (N 2 - восстановитель)
Эти реакции в обычных условиях не протекают. С фтором и другими галогенами азот непосредственно не взаимодействует, а с кислородом реакция происходит при температуре электрических искровых разрядов:
N 2 + О 2 = 2NO
Реакция сильно обратимая; прямая протекает с поглощением тепла (эндотермичная).
АЗОТ
N
(nitrogenium)
,
химический элемент (ат. номер 7) VA подгруппы периодической системы элементов. Атмосфера Земли содержит 78% (об.) азота. Чтобы показать, как велики эти запасы азота, отметим, что в атмосфере над каждым квадратным километром земной поверхности находится столько азота, что из него можно получить до 50 млн. т нитрата натрия или 10 млн. т аммиака (соединение азота с водородом) и все же это составляет малую долю азота, содержащегося в земной коре. Существование свободного азота свидетельствует о его инертности и трудности взаимодействия с другими элементами при обычной температуре. Связанный азот входит в состав как органической, так и неорганической материи. Растительный и животный мир содержит азот, связанный с углеродом и кислородом в белках. Помимо этого известны и могут быть получены в больших количествах азотсодержащие неорганические соединения, такие, как нитраты (NO3-), нитриты (NO2-), цианиды (CN-), нитриды (N3-) и азиды (N3-).
Историческая справка.
Опыты А. Лавуазье, посвященные исследованию роли атмосферы в поддержании жизни и процессов горения, подтвердили существование относительно инертного вещества в атмосфере. Не установив элементную природу остающегося после сгорания газа, Лавуазье назвал его azote, что на древнегреческом означает "безжизненный". В 1772 Д.Резерфорд из Эдинбурга установил, что этот газ является элементом, и назвал его "вредный воздух". Латинское название азота происходит от греческих слов nitron и gen, что означает "образующий селитру".
Фиксация азота и азотный цикл.
Термин "фиксация азота" означает процесс связывания атмосферного азота N2. В природе это может происходить двумя путями: либо бобовые растения, например горох, клевер и соя, накапливают на своих корнях клубеньки, в которых бактерии, фиксирующие азот, превращают его в нитраты, либо происходит окисление атмосферного азота кислородом в условиях разряда молнии. С.Аррениус установил, что таким способом фиксируется до 400 млн. т азота ежегодно.
В атмосфере оксиды азота соединяются с дождевой водой, образуя азотную и азотистую кислоты. Кроме того, установлено, что с дождем и снегом на каждый гектар земли попадает ок. 6700 г азота; достигая почвы, они превращаются в нитриты и нитраты. Растения используют нитраты для образования растительных белковых веществ. Животные, питаясь этими растениями, усваивают белковые вещества растений и превращают их в животные белки. После смерти животных и растений происходит их разложение, азотные соединения превращаются в аммиак. Аммиак используется двумя путями: бактерии, не образующие нитратов, разрушают его до элементов, выделяя азот и водород, а другие бактерии образуют из него нитриты, которые другими бактериями окисляются до нитратов. Таким образом происходит круговорот азота в природе, или азотный цикл.
Строение ядра и электронных оболочек.
В природе существуют два стабильных изотопа азота: с массовым числом 14 (N содержит 7 протонов и 7 нейтронов) и с массовым числом 15 (содержит 7 протонов и 8 нейтронов). Их соотношение составляет 99,635:0,365, поэтому атомная масса азота равна 14,008. Нестабильные изотопы азота 12N, 13N, 16N, 17N получены искусственно. Схематически электронное строение атома азота таково: 1s22s22px12py12pz1. Следовательно, на внешней (второй) электронной оболочке находится 5 электронов, которые могут участвовать в образовании химических связей; орбитали азота могут также принимать электроны, т.е. возможно образование соединений со степенью окисления от (-III) до (V), и они известны.
См. также АТОМА СТРОЕНИЕ .
Молекулярный азот.
Из определений плотности газа установлено, что молекула азота двухатомна, т.е. молекулярная формула азота имеет вид NєN (или N2). У двух атомов азота три внешних 2p-электрона каждого атома образуют тройную связь:N:::N:, формируя электронные пары. Измеренное межатомное расстояние N-N равно 1,095 . Как и в случае с водородом (см. ВОДОРОД), существуют молекулы азота с различным спином ядра - симметричные и антисимметричные. При обычной температуре соотношение симметричной и антисимметричной форм равно 2:1. В твердом состоянии известны две модификации азота: a - кубическая и b - гексагональная с температурой перехода a (r) b -237,39° С. Модификация b плавится при -209,96° С и кипит при -195,78° C при 1 атм (см. табл. 1). Энергия диссоциации моля (28,016 г или 6,023*10 23 молекул) молекулярного азота на атомы (N2 2N) равна примерно -225 ккал. Поэтому атомарный азот может образовываться при тихом электрическом разряде и химически более активен, чем молекулярный азот.
Получение и применение.
Способ получения элементного азота зависит от требуемой его чистоты. В огромных количествах азот получают для синтеза аммиака, при этом допустимы небольшие примеси благородных газов.
Азот из атмосферы.
Экономически выделение азота из атмосферы обусловлено дешевизной метода сжижения очищенного воздуха (пары воды, CO2, пыль, другие примеси удалены). Последовательные циклы сжатия, охлаждения и расширения такого воздуха приводят к его сжижению. Жидкий воздух подвергают фракционной перегонке при медленном подъеме температуры. Первыми выделяются благородные газы, затем азот, и остается жидкий кислород. Очистка достигается многократностью процессов фракционирования. Таким методом производят многие миллионы тонн азота ежегодно, преимущественно для синтеза аммиака, который является исходным сырьем в технологии производства различных азотсодержащих соединений для промышленности и сельского хозяйства. Кроме того, очищенную азотную атмосферу часто используют, когда недопустимо присутствие кислорода.
Лабораторные способы.
Азот в небольших количествах можно получать в лаборатории разными способами, окисляя аммиак или ион аммония, например:

Очень удобен процесс окисления иона аммония нитрит-ионом:
Известны и другие способы - разложение азидов при нагревании, разложение аммиака оксидом меди(II), взаимодействие нитритов с сульфаминовой кислотой или мочевиной:

При каталитическом разложении аммиака при высокой температуре тоже можно получить азот:
Физические свойства.
Некоторые физические свойства азота приведены в табл. 1.
Таблица 1. НЕКОТОРЫЕ ФИЗИЧЕСКИЕ СВОЙСТВА АЗОТА
Плотность, г/см3 0,808 (жидк.) Температура плавления, ° С -209,96 Температура кипения, ° С -195,8 Критическая температура, ° С -147,1 Критическое давление, атма 33,5 Критическая плотность, г/см3 а 0,311 Удельная теплоемкость, Дж/(мольЧК) 14,56 (15° С) Электроотрицательность по Полингу 3 Ковалентный радиус, 0,74 Кристаллический радиус, 1,4 (M3-) Потенциал ионизации, Вб
первый 14,54 второй 29,60
а
Температура и давление, при которых плотности азота жидкого и газообразного состояния одинаковы.
б
Количество энергии, необходимое для удаления первого внешнего и следующего за ним электронов, в расчете на 1 моль атомарного азота.
Химические свойства. Как уже было отмечено, преобладающим свойством азота при обычных условиях температуры и давления является его инертность, или малая химическая активность. Электронная структура азота содержит электронную пару на 2s-уровне и три наполовину заполненные 2р-орбитали, поэтому один атом азота может связывать не более четырех других атомов, т.е. его координационное число равно четырем. Небольшой размер атома также ограничивает количество атомов или групп атомов, которые могут быть связаны с ним. Поэтому многие соединения других членов подгруппы VA либо вовсе не имеют аналогов среди соединений азота, либо аналогичные соединения азота оказываются нестабильными. Так, PCl5 - стабильное соединение, а NCl5 не существует. Атом азота способен связываться с другим атомом азота, образуя несколько достаточно стабильных соединений, такие, как гидразин N2H4 и азиды металлов MN3. Такой тип связи необычен для химических элементов (за исключением углерода и кремния). При повышенных температурах азот реагирует со многими металлами, образуя частично ионные нитриды MxNy. В этих соединениях азот заряжен отрицательно. В табл. 2 приведены степени окисления и примеры соответствующих соединений.
Таблица 2. СТЕПЕНИ ОКИСЛЕНИЯ АЗОТА И СООТВЕТСТВУЮЩИЕ СОЕДИНЕНИЯ
Степень окисления Примеры соединений
-III Аммиак NH3, ион аммония NH4+, нитриды M3N2 -II Гидразин N2H4 -I Гидроксиламин NH2OH I Гипонитрит натрия Na2N2O2, оксид азота(I) N2O II Оксид азота(II) NO III Оксид азота(III) N2O3, нитрит натрия NaNO2 IV Оксид азота(IV) NO2, димер N2O4 V Оксид азота(V) N2O5, азотная кислота HNO3 и ее соли (нитраты) Нитриды. Соединения азота с более электроположительными элементами, металлами и неметаллами - нитриды, - похожи на карбиды и гидриды. Их можно разделить в зависимости от характера связи M-N на ионные, ковалентные и с промежуточным типом связи. Как правило, это кристаллические вещества.
Ионные нитриды. Связь в этих соединениях предполагает переход электронов от металла к азоту с образованием иона N3-. К таким нитридам относятся Li3N, Mg3N2, Zn3N2 и Cu3N2. Кроме лития, другие щелочные металлы IA подгруппы нитридов не образуют. Ионные нитриды имеют высокие температуры плавления, реагируют с водой, образуя NH3 и гидроксиды металлов.
Ковалентные нитриды. Когда электроны азота участвуют в образовании связи совместно с электронами другого элемента без перехода их от азота к другому атому, образуются нитриды с ковалентной связью. Нитриды водорода (например, аммиак и гидразин) полностью ковалентны, как и галогениды азота (NF3 и NCl3). К ковалентным нитридам относятся, например, Si3N4, P3N5 и BN - высокостабильные белые вещества, причем BN имеет две аллотропные модификации: гексагональную и алмазоподобную. Последняя образуется при высоких давлениях и температурах и имеет твердость, близкую к твердости алмаза.
Нитриды с промежуточным типом связи. Переходные элементы в реакции с NH3 при высокой температуре образуют необычный класс соединений, в которых атомы азота распределены между регулярно расположенными атомами металла. В этих соединениях нет четкого смещения электронов. Примеры таких нитридов - Fe4N, W2N, Mo2N, Mn3N2. Эти соединения, как правило, совершенно инертны и обладают хорошей электрической проводимостью.
Водородные соединения азота. Азот и водород взаимодействуют, образуя соединения, отдаленно напоминающие углеводороды (см. также ОРГАНИЧЕСКАЯ ХИМИЯ). Стабильность азотоводородов уменьшается с увеличением числа атомов азота в цепи в отличие от углеводородов, которые устойчивы и в длинных цепях. Наиболее важные нитриды водорода - аммиак NH3 и гидразин N2H4. К ним относится также азотистоводородная кислота HNNN (HN3).
Аммиак NH3. Аммиак - один из наиболее важных промышленных продуктов современной экономики. В конце 20 в. США производили ок. 13 млн. т аммиака ежегодно (в пересчете на безводный аммиак).
Строение молекулы. Молекула NH3 имеет почти пирамидальное строение. Угол связи H-N-H составляет 107°, что близко к величине тетраэдрического угла 109°. Неподеленная электронная пара эквивалентна присоединенной группе, в результате координационное число азота равно 4 и азот располагается в центре тетраэдра.

Cвойства аммиака.
Некоторые физические свойств аммиака в сравнении с водой приведены в табл. 3.
Таблица 3. НЕКОТОРЫЕ ФИЗИЧЕСКИЕ СВОЙСТВА АММИАКА И ВОДЫ
Температуры кипения и плавления у аммиака намного ниже, чем у воды, несмотря на близость молекулярных масс и сходство строения молекул. Это объясняется относительно большей прочностью межмолекулярных связей у воды, чем у аммиака (такая межмолекулярная связь называется водородной).
Аммиак как растворитель. Высокая диэлектрическая проницаемость и дипольный момент жидкого аммиака позволяют использовать его как растворитель для полярных или ионных неорганических веществ. Аммиак-растворитель занимает промежуточное положение между водой и органическими растворителями типа этилового спирта. Щелочные и щелочноземельные металлы растворяются в аммиаке, образуя темносиние растворы. Можно полагать, что в растворе происходит сольватация и ионизация валентных электронов по схеме
Синий цвет связывают с сольватацией и движением электронов или с подвижностью "дырок" в жидкости. При высокой концентрации натрия в жидком аммиаке раствор принимает бронзовую окраску и отличается высокой электропроводностью. Несвязанный щелочной металл можно выделить из такого раствора испарением аммиака или добавлением хлорида натрия. Растворы металлов в аммиаке являются хорошими восстановителями. В жидком аммиаке происходит автоионизация
![]()
аналогично процессу, протекающему в воде
![]()
Некоторые химические свойства обеих систем сопоставлены в табл. 4. Жидкий аммиак как растворитель имеет преимущество в некоторых случаях, когда невозможно проводить реакции в воде из-за быстрого взаимодействия компонентов с водой (например, окисление и восстановление). Например, в жидком аммиаке кальций реагирует с KCl с образованием CaCl2 и K, поскольку CaCl2 нерастворим в жидком аммиаке, а К растворим, и реакция протекает полностью. В воде такая реакция невозможна из-за быстрого взаимодействия Ca с водой. Получение аммиака. Газообразный NH3 выделяется из солей аммония при действии сильного основания, например, NaOH:
Метод применим в лабораторных условиях. Небольшие производства аммиака основаны также на гидролизе нитридов, например Mg3N2, водой. Цианамид кальция CaCN2 при взаимодействии с водой также образует аммиак. Основным промышленным методом получения аммиака является каталитический синтез его из атмосферного азота и водорода при высоких температуре и давлении:

Водород для этого синтеза получают термическим крекингом углеводородов, действием паров воды на уголь или железо, разложением спиртов парами воды или электролизом воды. На синтез аммиака получено множество патентов, отличающихся условиями проведения процесса (температура, давление, катализатор). Существует способ промышленного получения при термической перегонке угля. С технологической разработкой синтеза аммиака связаны имена Ф.Габера и К.Боша.
Химические свойства аммиака.
Кроме реакций, упомянутых в табл. 4, аммиак реагирует с водой, образуя соединение NH3ЧH2O, которое часто ошибочно считают гидроксидом аммония NH4OH; в действительности существование NH4OH в растворе не доказано. Водный раствор аммиака ("нашатырный спирт") состоит преимущественно из NH3, H2O и малых концентраций ионов NH4+ и OH-, образующихся при диссоциации
Основной характер аммиака объясняется наличием неподеленной электронной пары азота:NH3. Поэтому NH3 - это основание Льюиса, которое имеет высшую нуклеофильную активность, проявляемую в форме ассоциации с протоном, или ядром атома водорода:
Любые ион или молекула, способные принимать электронную пару (электрофильное соединение), будут взаимодействовать с NH3 с образованием координационного соединения. Например:

Символ Mn+ представляет ион переходного металла (B-подгруппы периодической таблицы, например, Cu2+, Mn2+ и др.). Любая протонная (т.е. Н-содержащая) кислота реагирует с аммиаком в водном растворе с образованием солей аммония, таких, как нитрат аммония NH4NO3, хлорид аммония NH4Cl, сульфат аммония (NH4)2SO4, фосфат аммония (NH4)3PO4. Эти соли широко применяются в сельском хозяйстве как удобрения для введения азота в почву. Нитрат аммония кроме того применяют как недорогое взрывчатое вещество; впервые оно было применено с нефтяным топливом (дизельным маслом). Водный раствор аммиака применяют непосредственно для введения в почву или с орошающей водой. Мочевина NH2CONH2, получаемая синтезом из аммиака и углекислого газа, также является удобрением. Газообразный аммиак реагирует с металлами типа Na и K с образованием амидов:
Аммиак реагирует с гидридами и нитридами также с образованием амидов:

Амиды щелочных металлов (например, NaNH2) реагируют с N2O при нагревании, образуя азиды:
Газообразный NH3 восстанавливает оксиды тяжелых металлов до металлов при высокой температуре, по-видимому, благодаря водороду, образующемуся в результате разложения аммиака на N2 и H2:
Атомы водорода в молекуле NH3 могут замещаться на галоген. Иод реагирует с концентрированным раствором NH3, образуя смесь веществ, содержащую NI3. Это вещество очень неустойчиво и взрывается при малейшем механическом воздействии. При реакции NH3 c Cl2 образуются хлорамины NCl3, NHCl2 и NH2Cl. При воздействии на аммиак гипохлорита натрия NaOCl (образуется из NaOH и Cl2) конечным продуктом является гидразин:

Гидразин.
Приведенные выше реакции представляют собой способ получения моногидрата гидразина состава N2H4ЧH2O. Безводный гидразин образуется при специальной перегонке моногидрата с BaO или другими водоотнимающими веществами. По свойствам гидразин слегка напоминает пероксид водорода H2O2. Чистый безводный гидразин - бесцветная гигроскопичная жидкость, кипящая при 113,5° C; хорошо растворяется в воде, образуя слабое основание
В кислой среде (H+) гидразин образует растворимые соли гидразония типа []+X-. Легкость, с которой гидразин и некоторые его производные (например, метилгидразин) реагируют с кислородом, позволяет использовать его в качестве компонента жидкого ракетного топлива. Гидразин и все его производные сильно ядовиты. Оксиды азота. В соединениях с кислородом азот проявляет все степени окисления, образуя оксиды: N2O, NO, N2O3, NO2 (N2O4), N2O5. Имеется скудная информация об образовании пероксидов азота (NO3, NO4). Оксид азота(I) N2O (монооксид диазота) получается при термической диссоциации нитрата аммония:
Молекула имеет линейное строение
N2O довольно инертен при комнатной температуре, но при высоких температурах может поддерживать горение легко окисляющихся материалов. N2O, известный как "веселящий газ", используют для умеренной анестезии в медицине. Оксид азота(II) NO - бесцветный газ, является одним из продуктов каталитической термической диссоциации аммиака в присутствии кислорода:
![]()
NO образуется также при термическом разложении азотной кислоты или при реакции меди с разбавленной азотной кислотой:
NO можно получать синтезом из простых веществ (N2 и O2) при очень высоких температурах, например, в электрическом разряде. В структуре молекулы NO имеется один неспаренный электрон. Соединения с такой структурой взаимодействуют с электрическим и магнитным полями. В жидком или твердом состоянии оксид имеет голубую окраску, поскольку неспаренный электрон вызывает частичную ассоциацию в жидком состоянии и слабую димеризацию в твердом состоянии: 2NO N2O2. Оксид азота(III) N2O3 (триоксид азота) - ангидрид азотистой кислоты: N2O3 + H2O 2HNO2. Чистый N2O3 может быть получен в виде голубой жидкости при низких температурах (-20° С) из эквимолекулярной смеси NO и NO2. N2O3 устойчив только в твердом состоянии при низких температурах (т.пл. -102,3° С), в жидком и газообразном состояния он снова разлагается на NO и NO2. Оксид азота(IV) NO2 (диоксид азота) также имеет в молекуле неспаренный электрон (см. выше оксид азота(II)). В строении молекулы предполагается трехэлектронная связь, и молекула проявляет свойства свободного радикала (одна линия соответствует двум спаренным электронам):

NO2 получается каталитическим окислением аммиака в избытке кислорода или окислением NO на воздухе:

а также по реакциям:

При комнатной температуре NO2 - газ темнокоричневого цвета, обладает магнитными свойствами благодаря наличию неспаренного электрона. При температурах ниже 0° C молекула NO2 димеризуется в тетраоксид диазота, причем при -9,3° C димеризация протекает полностью: 2NO2 N2O4. В жидком состоянии недимеризовано только 1% NO2, а при 100° C остается в виде димера 10% N2O4. NO2 (или N2O4) реагирует в теплой воде с образованием азотной кислоты: 3NO2 + H2O = 2HNO3 + NO. Технология NO2 поэтому очень существенна как промежуточная стадия получения промышленно важного продукта - азотной кислоты. Оксид азота(V) N2O5 (устар. ангидрид азотной кислоты) - белое кристаллическое вещество, получается обезвоживанием азотной кислоты в присутствии оксида фосфора P4O10:
![]()
N2O5 легко растворяется во влаге воздуха, вновь образуя HNO3. Свойства N2O5 определяются равновесием

N2O5 - хороший окислитель, легко реагирует, иногда бурно, с металлами и органическими соединениями и в чистом состоянии при нагреве взрывается. Вероятную структуру N2O5 можно представить как

Оксокислоты азота.
Для азота известны три оксокислоты: гипоазотистая H2N2O2, азотистая HNO2 и азотная HNO3. Гипоазотистая кислота H2N2O2 - очень нестабильное соединение, образуется в неводной среде из соли тяжелого металла - гипонитрита при действии другой кислоты: M2N2O2 + 2HX 2MX + H2N2O2. При выпаривании раствора образуется белое взрывчатое вещество с предполагаемой структурой H-O-N=N-O-H.
Азотистая кислота HNO2 не существует в чистом виде, однако водные растворы ее невысокой концентрации образуются при добавлении серной кислоты к нитриту бария:
Азотистая кислота образуется также при растворении эквимолярной смеси NO и NO2 (или N2O3) в воде. Азотистая кислота немного сильнее уксусной кислоты. Степень окисления азота в ней +3 (ее структура H-O-N=O), т.е. она может являться и окислителем, и восстановителем. Под действием восстановителей она восстанавливается обычно до NO, а при взаимодействии с окислителями окисляется до азотной кислоты. Скорость растворения некоторых веществ, например металлов или иодид-иона, в азотной кислоте зависит от концентрации азотистой кислоты, присутствующей в виде примеси. Соли азотистой кислоты - нитриты - хорошо растворяются в воде, кроме нитрита серебра. NaNO2 применяется в производстве красителей. Азотная кислота HNO3 - один из наиболее важных неорганических продуктов основной химической промышленности. Она используется в технологиях множества других неорганических и органических веществ, например, взрывчатых веществ, удобрений, полимеров и волокон, красителей, фармацевтических препаратов и др.
См. также
ЭЛЕМЕНТЫ ХИМИЧЕСКИЕ .
ЛИТЕРАТУРА
Справочник азотчика. М., 1969 Некрасов Б.В. Основы общей химии. М., 1973 Проблемы фиксации азота. Неорганическая и физическая химия. М., 1982
Энциклопедия Кольера. - Открытое общество . 2000 .
Синонимы :Смотреть что такое "АЗОТ" в других словарях:
- (N) химический элемент, газ, без цвета, вкуса и запаха; составляет 4/5 (79 %) воздуха; уд. вес 0,972; атомный вес 14; сгущается в жидкость при 140 °С. и давлении 200 атмосфер; составная часть многих растительных и животных веществ. Словарь… … Словарь иностранных слов русского языка
АЗОТ - АЗОТ, хим. элемент, симв. N (франц. AZ), порядковый номер 7, ат. в. 14,008; точка кипения 195,7°; 1 л А. при 0° и 760 мм давл. весит 1,2508 г [лат. Nitrogenium («порождающий селитру»), нем. Stickstoff («удушающее… … Большая медицинская энциклопедия
- (лат. Nitrogenium) N, химический элемент V группы периодической системы, атомный номер 7, атомная масса 14,0067. Название от греческой a отрицательная приставка и zoe жизнь (не поддерживает дыхания и горения). Свободный азот состоит из 2 атомных… … Большой Энциклопедический словарь
азот - а м. azote m. <араб. 1787. Лексис.1. алхим. Первая материя металлов металлическая ртуть. Сл. 18. Пустился он <парацельс> на конец по свету, предлагая всем за весьма умеренную цену свой Лауданум и свой Азот, для изцеления всех возможных… … Исторический словарь галлицизмов русского языка
- (Nitrogenium), N, химический элемент V группы периодической системы, атомный номер 7, атомная масса 14,0067; газ, tкип 195,80 шС. Азот основной компонент воздуха (78,09% по объему), входит в состав всех живых организмов (в организме человека… … Современная энциклопедия
Азот - (Nitrogenium), N, химический элемент V группы периодической системы, атомный номер 7, атомная масса 14,0067; газ, tкип 195,80 °С. Азот основной компонент воздуха (78,09% по объему), входит в состав всех живых организмов (в организме человека… … Иллюстрированный энциклопедический словарь
- (хим. знак N, атомный вес 14) один из химических элементов;бесцветный газ, не имеющий ни запаха, ни вкуса; очень мало растворим вводе. Удельный вес его 0.972. Пикте в Женеве и Кальете в Париже удалосьсгустить азот, подвергая его высокому давлению … Энциклопедия Брокгауза и Ефрона
АЗОТ , N (франц. Az), химический элемент (Nitrogenium - от nitrum, селитра, «образующий селитру»; по-немецки - Stickstoff «удушающий газ», по-франц. - Azote, от греч. α - отрицание, ξωη - жизнь, безжизненный); атомный вес 14,009, порядковый номер 7.
Физические свойства . D чистого азота (при D воздуха = 1) 0,9674; но обычно мы имеем дело с азотом из воздуха, с содержанием 1,12% аргона, D такого азота 0,9721; вес 1 л чистого азота при 0°С и 760 мм - 1,2507 г, вес 1 л «атмосферного» азота - 1,2567 г. Растворимость азота в воде меньше растворимости кислорода. 1 л воды при 760 мм и 0°С растворяет 23,5 см 3 азота (растворимость О 2 - 48,9 см 3), при 20°С - 15,4 см 3 азота (растворимость О 2 - 31,0 см 3). Древесный уголь свежепрокаленный поглощает, по Дьюару, в 1 см 3 при 0°С всего 15 см 3 азота, при -185°С он поглощает 155 см 3 азота (объемы перечислены на 0°С и 760 мм). Температура критическая -147°С при критическом давлении в 33 atm., или 25 м ртутного столба, температура кипения при 760 мм равна -195°,67±0°,05, а температура плавления при 88 мм±4 мм равна - 210°,52±0°,2. Коэффициент расширения азота при 1 atm равен 0,003667; удельная теплота при 20°С равна 0,249, а для температурного интервала (0-1400)°С, в среднем, 0,262; отношение с р /с η = 1,40, как и для О 2 . Жидкий азот бесцветен, подвижен как вода, хотя легче последней. Удельный вес при температуре кипения и 760 мм - 0,7914, при -184°С - 0,7576, при -195,5°С - 0,8103 и при -205°С - 0,8537; близ точки застывания - 0,8792 (цифры колеблются в зависимости от содержания Аr). Удельная теплота жидкого азота между -196°С и -208°С - 0,430; теплота испарения 1кг жидкого азота при температуре кипения -195°,55 равна 47,65 Cal. Из 1 л жидкого азота при испарении, при атмосферном давлении и 0°С, 14°С и 27°С, образуется соответственно: 640, 670 и 700 л газообразного азота. Жидкий азот немагнитен и не проводит электричества.
Химические свойства азота в значительной степени определяются его крайней инертностью при обыкновенных условиях температуры и давления, объясняющеюся устойчивостью молекул N 2 . Только металл литий соединяется с азотом при невысокой температуре, выделяя при этом 69000 cal и образуя нитрид лития NLi 3 . Нитрид Ва образуется при 560°С и имеет формулу Ba 3 N 2 ; о других нитридах. Как с кислородом, так и с водородом азот соединяется лишь при высокой температуре, причем реакция с кислородом эндотермична, а с водородом экзотермична. Валентность азота определяется строением его атома по Бору. При удалении с наружного кольца всех пяти электронов азот становится пятизарядным положительным ионом; при пополнении верхнего кольца тремя электронами до предельного числа - восьми - атом азота проявляется как трехзарядный электроотрицательный ион. Состояние азота в аммонийных соединениях может быть легко выяснено теорией комплексных соединений. Азот дает целый ряд соединений с кислородом и с галоидами (последние соединения являются вследствие сильной эндотермичности своего образования чрезвычайно взрывчатыми). С водородом азот дает соединения: аммиак и азотистоводородную кислоту. Кроме того, известны: соединение азота с водородом - гидразин и с водородом и кислородом - гидроксиламин.
Применение азота . Газообразный азот имеет в качестве инертного газа применение в медицине для иммобилизации пораженных туберкулезом участков легких (операция Pneumotorax), для защиты металлов от химического действия на них активных газов и вообще в тех случаях, когда необходимо предотвратить какую-нибудь нежелательную химическую реакцию (например, для наполнения лампочек накаливания, для надувания автомобильных резиновых шин, на которые при высоком давлении разрушающим образом действует воздух, для сохранения красок ценных картин, помещаемых в наполненных азотом герметических сосудах, для предотвращения пожарной опасности при переливке бензина и других горючих жидкостей, и т. п.). Но самое важное техническое применение азота имеет в процессе получения синтетического аммиака из элементов.
При оценке свойств азота и его исключительного значения в общей экономике органической природы и общественной жизни человека следует резко различать азот свободный от азота связанного , т. е. уже вступившего в химическое соединение с каким-нибудь другим элементом, гл. обр. с кислородом, водородом и углеродом . Азот свободный при условиях температуры и давления, господствующих на поверхности земного шара, представляет собою крайне инертный элемент. Мышь в классическом опыте Лавуазье погибала в воздухе, лишенном кислорода, т. е. в почти чистом азоте. Между тем связанный азот является как бы носителем жизни, ибо все без исключения живые существа, будь это растения или животные, выстраивают свой организм обязательно при участии т. н. белковых веществ, неизбежно заключающих в своем химическом составе азот (белки содержат до 16% азота). Процесс перехода от свободного азота к связанному и обратно представляет собою величайшей важности процесс природы и грандиознейшую проблему сельского хозяйства, а в последнее время и индустрии. Свободный азот содержится в смеси с другими газами в атмосфере в необъятном количестве, составляя около 4 / 5 по объему (75,51 весовых %) от всей атмосферы и окутывая земной шар воздушным покровом, постепенно все более и более разрежающимся, достигающим в высоту десятков км. Над одним гектаром земной поверхности содержится азота столько, что, если бы он был в связанном состоянии, его хватило бы для обеспечения всей живой природы и потребностей человечества на 20 лет (А. Э. Мозер). Но свободный азот лишь с громадным усилием м. б. понужден к соединению с другими элементами, и притом не только в тех случаях, когда это соединение происходит эндотермически (как, например, при образовании кислородных соединений азота), но и в тех случаях, когда соединение азота с другим элементом сопровождается выделением энергии и является реакцией экзотермической (соединение азота с водородом).
Лишь в исключительных случаях, например, с литием, соединение азота протекает в обыкновенных условиях температуры и давления легко. Поэтому в общем балансе связанного азота в природе приходится констатировать круговорот . Растения поглощают связанный азот в виде растворимых солей из почвы и изготовляют белки; животные пользуются при обмене веществ готовыми азотистыми соединениями за счет поглощенной растительной пищи, выделяя соединения связанного азота, неусвоенные, а также образовавшиеся в результате распада в их организме белковых веществ - в экскрементах и в моче, и, наконец, внося при своей гибели весь свой организм в общий баланс связанного азота в природе для дальнейших процессов минерализации белковых и других азотистых веществ, происходящих в почве. В этих последних процессах громадная роль остается за микроорганизмами почвы, в результате жизнедеятельности которых сложные азотистые органические соединения превращаются в простейшие соли азотной кислоты, которая, в свою очередь, образуется в результате окисления в почве аммиачных соединений как более ранней стадии разрушения белковых веществ и продуктов ид распада. Принимая во внимание чрезвычайную инертность свободного азота, неспособного самостоятельно вступать в соединения, и, с другой стороны, потери или случаи глубокого разрушения азотистого соединения до свободного азота (например, в результате жизнедеятельности денитрифицирующих почвенных бактерий, при сжигании каменного угля , дров и торфа, при вымывании из почвы азотистых соединений дождем в реки и моря, при спуске в реки отбросов больших городов и т. д.), - можно было бы считать неизбежным последствием всего этого постепенное обеднение природы связанным азотом и в результате гибель органической жизни на земле, если бы в общее русло круговорота связанного азота не вливались бы некоторые процессы, пополняющие указанную убыль связанного азота в природе. Таким естественным источником связанного азота в природе являются атмосферные осадки, приносящие в почву окислы азота, образовавшиеся в атмосфере при электрических разрядах, которые понуждают некоторое количество атмосферного азота соединиться с кислородом (дождевая вода содержит около 0,00001% связанного азота). Можно подсчитать, что этим путем в почву земного шара ежегодно вносится до 400 млн. т связанного азота. Кроме того, Бертело удалось установить, что в почве, без внесения в нее новых запасов азотистых соединений, содержание азота с течением времени повышается благодаря жизнедеятельности некоторых видов бактерий. Впоследствии эти бактерии были выделены в чистых культурах, а именно: анаэробная бактерия маслянокислого брожения (Clostridium pasteuri- anum) и аэробная бактерия (Azotobakter Виноградского, которая может обогатить почву на 48 кг в год на 1 га). Кроме этих свободно живущих в почве бактерий, было обнаружено в клубеньковых наростах некоторых растений семейства бобовых (Leguminosae) присутствие симбиотически связанных с ними бактерий (Bacillus radicicola), также способных усваивать свободный атмосферный азот и передавать этот связанный ими азот своему «растению-хозяину». Как известно, это свойство бобовых растений (лупина, вики, сераделлы и др.) широко применяется для обогащения почвы азотистыми веществами, являясь своеобразным методом удобрения почвы для последующих посевов хлебных злаков на участке с запаханными и разложившимися в почве, предварительно взращенными на ней, удобрительными растениями. Однако указанные естественные источники пополнения связанного азота в природе никоим образом не могут восполнить его убыли, в особенности в виду громадного расточения связанного азота во всех процессах разрушения азотистых соединений в топливе, а также при использовании азотистых взрывчатых веществ. Принимая во внимание потребности в азотистой пище населения земли, исчисляемого в 1,6 млрд. чел., и ежегодный прирост населения земли в одних только странах, располагающих статистическими сведениями, в 4 млн. чел. или в 400 млн. в столетие, эту убыль связанного азота в природе приходится считать весьма существенной. Вильям Крукс еще в 1898 г. забил тревогу, предсказывая гибель человечества от голода в ближайшем будущем, когда, по его расчетам, должны будут иссякнуть единственные на земном шаре богатые месторождения чилийской селитры - того ресурса связанного азота, который гл. обр. должен был восполнить насущную нужду сельского хозяйства в азотных удобрениях, а вместо того хищнически расточался для военных целей, т. к. большинство взрывчатых веществ изготовлялось при действии азотной кислоты, полученной из чилийской селитры. Действительно, хотя Крукс преуменьшил несколько запасы селитры в Чили, однако и по последним геологическим подсчетам, если даже принять только довоенную норму выработки чилийской селитры (2750000 т селитры с содержанием 400000 т связанного азота), ее запасов (600 млн. т селитры с содержанием 30 млн. т связанного азота) не может хватить более, чем на 150-200 лет (см. Селитра). Однако запасы чилийской селитры отнюдь не являются единственным источником, из которого человечество черпает свои пополнения необходимого для его питания и промышленности связанного азота. По данным Интернационального агрикультурного института в Риме, вычисленным на основании сведений об урожаях всех стран света, мировое потребление связанного азота на 1924 г. определяется количеством около 7000000 т связанного азота; из них человек сумел выработать и вернуть природе лишь около 1 / 6 части, т. е. около 1200000 т связанного азота. На долю чилийской селитры в этом количестве пришлось в 1924 г. всего 420000 т. Остальное количество связанного азота поступило в общую экономику природы в значительной степени за счет таких же естественных ресурсов связанного азота в природе, как и селитра, требующих, однако, со стороны человека некоторой обработки. К числу таких естественных ресурсов связанного азота относятся мировые запасы каменного угля и торфа. Каменный уголь содержит даже в плохих сортах от 0,5 до 2% связанного азота. Те же сорта, которые идут для производства кокса и светильного газа, содержат обыкновенно от 1,2 до 1,9%, в среднем 1,3% связанного азота. По современным геологическим данным, мировые запасы каменного угля следует оценить приблизительной цифрой около 8000 млрд. т. Считая содержание связанного азота в угле в 1%, мы получим содержание связанного азота в мировом запасе каменного угля в 80 млрд. т, т. е. в 2000 раз больше, чем содержание связанного азота в запасах чилийской селитры. Это количество могло бы обеспечить потребность человечества в связанном азоте на 6000 лет, если бы при использовании угля можно было утилизировать весь заключающийся в нем связанный азот. Довоенная ежегодная выработка каменного угля была равна 1350 млн. т с содержанием связанного азота (1,3%) в 17 млн. т (соответственно 85 млн. т азотнокислого аммония, на сумму более 25 млрд. фр.). Однако почти все это количество связанного азота выпускалось в воздух в качестве свободного азота при сжигании каменного угля в печах заводов, паровозов, в домашних печах и т. д. Только примерно 1 / 50 ч. всего этого количества улавливалась азотной промышленностью и служила для получения сернокислого аммония, который является и поныне самым значительным, наравне с селитрой, ресурсом для искусственных азотных удобрений (Matignon). В среднем из каменного угля, подвергающегося коксованию или газации, добывается 12 кг сернокислого аммония на т. Утилизация связанного азота из торфа пока еще не представляет собою крупного фактора в экономике связанного азота. Т. о. использование каменноугольного азота только отчасти сглаживает остроту недостачи связанного азота для целей сельского хозяйства и промышленности, но отнюдь не является разрешением азотной проблемы в целом. Окончательное разрешение этой проблемы принесли с собой наука и техника, гл. обр. в продолжение текущего столетия, осуществив фиксацию атмосферного азота техническим путем. Эта фиксация осуществляется главным образом тремя основными методами: 1) путем сжигания азота воздуха при действии вольтовой дуги, с получением окислов азота и азотной кислоты; этот метод, вследствие эндотермичности реакции соединения N 2 + О 2 , требует затраты значительных количеств тепла, высокого напряжения, и является рентабельным только при наличии дешевой гидроэлектрической энергии; 2) путем присоединения азота при высокой температуре электрической печи к карбиду кальция, с образованием цианамида кальция; последний либо непосредственно идет для целей удобрения, либо при действии воды образует аммиак, нейтрализуемый до сернокислого или азотнокислого аммония; 3) путем непосредственного соединения атмосферного азота с водородом, с образованием синтетического аммиака; этот способ (Габер-Боша) является, несомненно, величайшим достижением химической технологии за истекшую часть 20 в. и одним из грандиознейших завоеваний науки и техники в истории человечества.
Несмотря на то, что для повышения урожая необходимо внесение в почву также и других удобрений - фосфорных и калийных, все же именно азотные удобрения играют преобладающее значение в экономике сельского хозяйства. Если, например, в мясе фосфорного ангидрида и окиси калия содержится по 0,4%, то количество связанного азота в том же продукте достигает около 3%, т. е. на 30 ч. связанного азота в мясе приходится лишь по 4 ч. Р 2 О 6 и К 2 О. При этом цены указанных трех видов искусственных удобрений в 1913 г., при нормальных, сравнительно, условиях довоенного времени, выражались следующими цифрами: за 1 кг связанного азота - 1,5 фр., а за 1 кг К 2 О или Р 2 О 5 - по 0,4 фр. за каждый. Т. о. мы можем считать, что азотные удобрения дают экономический эффект в 32 раза более значительный по сравнению с эффектом остальных двух классов удобрительных туков. Насколько значительна роль азотных удобрений, видно из того факта, что внесение в почву искусственных азотных удобрений вызывает, при прочих равных условиях, прирост урожая на 1 т внесенного связанного азота: для зерновых хлебов - в 20 т, для картофеля - в 200 т и для свеклы - в 300 т. Для количественной оценки роли вносимых в экономику сельского хозяйства азотистых удобрительных туков интересно хотя бы приблизительно подсчитать общий мировой капитал связанного азота, участвующий в органической жизни нашей планеты. При поверхности суши земного шара в 135000000 км 2 и толщине слоя пахотной земли в 0,4 м, мы можем оценить (приняв плотность почвы за единицу) весь капитал всей плодородной почвы земли в 54 млрд. т. Среднее содержание связанного азота в почве не превышает 0,1%. Уменьшив весь расчет до 3 / 4 вследствие учета пустынь, ледников, скал и других неплодородных почв, не содержащих азота, мы можем оценить общий тоннаж связанного азота в почве всего земного шара приблизительно в 40 млрд. т, т. е. в половину всех запасов связанного азота, имеющихся в каменном угле, утилизация которых возможна лишь в самой ограниченной степени.
Потребность мирового сельского хозяйства в азотных удобрительных туках характеризуется следующими цифрами (Partington, The Nitrogen Industry):

Мировое потребление чилийской селитры в военные годы мало показательно, ибо на нем отразились факторы блокады, затрудненного транспорта и пр.
Мировое производство связанного азота достигло 1200000 т в год, из которых: около 30% - 360000 т было выделено при коксовании и газификации из каменного угля, около 35% - 420000 т было выработано в виде чилийской селитры, около 35% - 420000 т было произведено путем фиксации атмосферного азота. В самые последние годы это соотношение несколько изменилось в смысле увеличения выработки селитры (до 36,5%) за счет уменьшения утилизации каменноугольного азота (около 30%).

Из всей продукции связанного азота путем фиксации атмосферного азота в свою очередь 60% д. б. отнесено к синтетическому аммиаку, 30% - к цианамиду и только 10% - к норвежской синтетической селитре. Особенно быстрое развитие азотной промышленности наблюдается в Германии, что характеризуется следующими цифрами: всего в Германии азотных продуктов было произведено: в 1915 г. - 64000 т связанного азота, в 1919 г. - 132000 т, в 1920 г. - 190000 т, в 1922 г. - 238000 т (в эти количества не входит ввезенная чилийская селитра). Следующая диаграмма наглядно рисует степень удовлетворения на 1925 г. мировой потребности в связанном азоте со стороны добывающей и обрабатывающей азотной промышленности.

Из всего количества добытого связанного азота 83% (около 1000000 т) было израсходовано для удобрения, вследствие чего был получен прирост сельскохозяйственных продуктов, эквивалентный 20000000 т (1,2 млрд. пудов) пшеницы, т. е. почти в два раза большего количества, чем весь хлебный годовой экспорт России в довоенные годы. Развитие синтетической азотной промышленности иллюстрируют следующие цифры:

По отдельным странам мировая производительная способность заводов, вырабатывающих соединения связанного азота, в 1925 г. подразделяется следующим образом (в т):

Т. о. в технической фиксации атмосферного азота по тому или иному методу участвуют: Германия на 60%, Франция - 14%, Англия - 2,5%, Италия - 4,3%, Япония - 1,9% и США - 18%. Но синтетическая азотная промышленность развивается чрезвычайно быстро. Уже в настоящее время частью заканчивается постройкой, а частью находится в действии целый ряд новых установок. Когда все они начнут функционировать, то общая продукция синтетического связанного азота будет еще больше.
Преобладающее значение и наибольшие перспективы из всех синтетических методов фиксации атмосферного азота следует признать за способами получения синтетического аммиака. Главным преимуществом этого пути фиксации атмосферного азота является весьма незначительная затрата энергии на его производство, ибо энергия, в виду экзотермичности процесса, д. б. затрачена, при рациональном использовании теплоты самой реакции, исключительно на компрессию газов до давления в 200 и более atm. Parsons (JournalofInd. a. Eng. Chem., v. 9, p. 839, 1917) приводит интересный подсчет расходуемой энергии на тонну связанного азота при разных методах:

Современное состояние синтетической аммиачной промышленности (на 1925 г.) характеризуется следующими цифрами:

Т. о. 93% всего синтетического аммиака производится в Германии. Когда все установки по фиксации атмосферного азота будут закончены, то количество производимого синтетического аммиака будет приблизительно равно, в переводе на тонну связанного азота:

В общем все виды технической фиксации атмосферного азота (аммиак, дуговой процесс и цианамидный метод) смогут дать ежегодную продукцию, вероятно несколько меньшую указанной выше, а именно:

В СССР выработано в 1924 г. около 7400 т концентрированной аммиачной воды с содержанием около 400 т связанного азота, кроме того было импортировано значительное количество чилийской селитры с содержанием 1700 т связанного азота. О потребностях СССР можно получить представление из следующих цифр. Во время войны Россией было израсходовано на производство взрывчатых веществ около 330000 т селитры с 48000 т связанного азота. Потребность в азотистых удобрениях для культур сахарной свекловицы, хлопка и других технических растений исчисляется десятками тысяч тонн, а потребность в удобрениях для крестьянского хозяйства - многими сотнями тыс. т связанного азота. Недостаток удобрений вызывает слабый урожай в СССР, в среднем с 1 га 6,5 ц хлеба и 98 ц свекловицы, против 24,5 ц хлеба и 327,5 ц свекловицы в странах Западной Европы, применяющих азотные и другие искусственные удобрения (Мозер). В настоящее время в СССР принимаются решительные меры для обеспечения развития азотной промышленности. См. .
ОПРЕДЕЛЕНИЕ
Азот - седьмой элемент Периодической таблицы. Обозначение - N от латинского «nitrogenium». Расположен во втором периоде, VА группе. Относится к неметаллам. Заряд ядра равен 7.
Большая часть азота находится в свободном состоянии. Свободный азот является главной составной частью воздуха, который содержит 78,2% (об.) азота. Неорганические соединения азота не встречаются в природе в больших количествах, если не считать натриевую селитру NaNO 3 , образующую мощные пласты на побережье Тихого океана в Чили. Почва содержит незначительные количества азота, преимущественно в виде солей азотной кислоты. Но в виде сложных органических соединений - белков - азот входит в состав всех живых организмов.
В виде простого вещества азот - это бесцветный газ, не имеющий запаха и весьма мало растворимый в воде. Он немного легче воздуха: масса 1 л азота равна 1,25 г.
Атомная и молекулярная масса азота
Относительной атомной массой элемента называют отношение массы атома данного элемента к 1/12 массы атома углерода. Относительная атомная масса безразмерна и обозначается A r (индекс «r» — начальная буква английского слова relative, что в переводе означает «относительный»). Относительная атомная масса атомарного азота равна 14,0064 а.е.м.
Массы молекул, также как массы атомов выражаются в атомных единицах массы. Молекулярной массой вещества называется масса молекулы, выраженная в атомных единицах массы. Относительной молекулярной массой вещества называют отношение массы молекулы данного вещества к 1/12 массы атома углерода, масса которого равна 12 а.е.м. Известно, что молекула азота двухатомна - N 2 . Относительная молекулярная масса молекулы азота будет равна:
M r (N 2) = 14,0064× 2 ≈ 28.
Изотопы азота
В природе азот существует в виде двух стабильных изотопов 14 N (99,635%) и 15 N (0,365%). Их массовые числа равны 14 и 15 соответственно. Ядро атома изотопа азота 14 N содержит семь протонов и семь нейтронов, а изотопа 15 N - такое же количество протонов и шесть нейтронов.
Существует четырнадцать искусственных изотопов азота с массовыми числами от 10-ти до 13-ти и от 16-ти до 25-ти, из которых наиболее стабильным является изотоп 13 Nс периодом полураспада равным 10 минут.
Ионы азота
На внешнем энергетическом уровне атома азота имеется пять электронов, которые являются валентными:
1s 2 2s 2 2p 3 .
Схема строения атома азота представлена ниже:
В результате химического взаимодействия азот может терять свои валентные электроны, т.е. являться их донором, и превращаться в положительно заряженные ионы или принимать электроны другого атома, т.е. являться их акцептором, и превращаться в отрицательно заряженные ионы:
N 0 -5e → N 2+ ;
N 0 -4e → N 4+ ;
N 0 -3e → N 3+ ;
N 0 -2e → N 2+ ;
N 0 -1e → N 1+ ;
N 0 +1e → N 1- ;
N 0 +2e → N 2- ;
N 0 +3e → N 3- .
Молекула и атом азота
Молекула азота состоит из двух атомов - N 2 . Приведем некоторые свойства, характеризующие атом и молекулу азота:
Примеры решения задач
ПРИМЕР 1
| Задание | Для образования хлорида аммония было взято 11,2 л (н.у.) газообразного аммиака и 11,4 л (н.у.) хлороводорода. Какова масса образовавшегося продукта реакции? |
| Решение | Запишем уравнение реакции получения хлорида аммония из аммиака и хлороводорода:
NH 3 + HCl = NH 4 Cl. Найдем количество молей исходных веществ: n(NH 3) = V(NH 3) / V m ; n(NH 3) = 11,2 / 22,4 = 0,5 моль. n(HCl) = V(NH 3) / V m ; n(HCl) = 11,4 / 22,4 = 0,51 моль. n(NH 3) n(NH 4 Cl) = n(NH 3) = 0,5 моль. Тогда, масса хлорида аммония будет равна: M(NH 4 Cl) = 14 + 4×1 + 35,5 = 53,5г/моль. m(NH 4 Cl) = n(NH 4 Cl) × M(NH 4 Cl); m(NH 4 Cl) = 0,5×53,5 = 26,75 г. |
| Ответ | 26,75 г |
ПРИМЕР 2
| Задание | 10,7 г хлорида аммония смешали с 6 г гидроксида кальция и смесь нагрели. Какой газ и сколько его по массе и объему выделилось (н.у.)? |
| Решение | Запишем уравнение реакции взаимодействия хлорида аммония с гидроксидом кальция:
2NH 4 Cl + Ca(OH) 2 = CaCl 2 + 2NH 3 - + 2H 2 O. Определим, какое из двух реагирующих веществ находится в избытке. Для этого рассчитаем их количество молей: M(NH 4 Cl) = A r (N) + 4×A r (H) + A r (Cl); M(NH 4 Cl) = 14 + 4×1 + 35,5 = 53,5 г/моль. n(NH 4 Cl) = m (NH 4 Cl) / M(NH 4 Cl); n(NH 4 Cl) = 10,7 / 53,5 = 0,1 моль. M(Ca(OH) 2) = A r (Ca) + 2×A r (H) + 2×A r (O); M(Ca(OH) 2) = 40 + 2×1 + 2×16 = 42 + 32 = 74 г/моль. n(Ca(OH) 2) = m (Ca(OH) 2) / M(Ca(OH) 2); n(Ca(OH) 2) = 6 / 74 = 0,08 моль. n(Ca(OH) 2) n(NH 3) = 2×n(Ca(OH) 2) = 2×0,08 = 0,16 моль. Тогда, масса аммиака будет равна: M(NH 3) = A r (N) + 3×A r (H) = 14 + 3×1 = 17 г/моль. m(NH 3) = n(NH 3) ×M(NH 3) = 0,16 × 17 = 2,72 г. Объем аммиака равен: V(NH 3) = n(NH 3) ×V m ; V(NH 3) = 0,16× 22,4 = 3,584 л. |
| Ответ | В результате реакции образовался аммиак объемом 3,584 л и массой 2,72 г. |